Wie können wir aus Rapsöl Biodiesel herstellen? - Umesterung von Rapsöl zu RME: Unterschied zwischen den Versionen
(→Der Weg zum Biodiesel auf molekularer Ebene) |
(→Habt ihr das richtige Edukt gefunden?) |
||
| Zeile 33: | Zeile 33: | ||
'''Material:''' Erlenmeyerkolben (250 mL) mit Stopfen, Becherglas (250 mL), Thermometer, Becherglas (1000 mL), Thermoskanne mit heißem Wasser | '''Material:''' Erlenmeyerkolben (250 mL) mit Stopfen, Becherglas (250 mL), Thermometer, Becherglas (1000 mL), Thermoskanne mit heißem Wasser | ||
| − | '''Durchführung:''' | + | '''Durchführung (Abzug! Gefahrensymbole auf dem AB beachten!):''' |
Schritt 1: Herstellung des Produkts | Schritt 1: Herstellung des Produkts | ||
Version vom 19. September 2018, 10:26 Uhr
Die begrenzte Verfügbarkeit fossiler Brennstoffe wie Diesel und Benzin ist nur einer der Gründe, weshalb an Tankstellen auch Biokraftstoffe zu finden sind. Biodiesel kann aus verschiedenen Pflanzenölen gewonnen werden, besonders häufig wird dazu Rapsöl verwendet. Mit den Informationen auf dieser Seite sollt ihr herausfinden, wie Biodiesel aus Rapsöl hergestellt werden kann und wie diese Umsetzung auf molekularer Ebene abläuft.
Inhaltsverzeichnis |
Die Struktur des Biodiesels
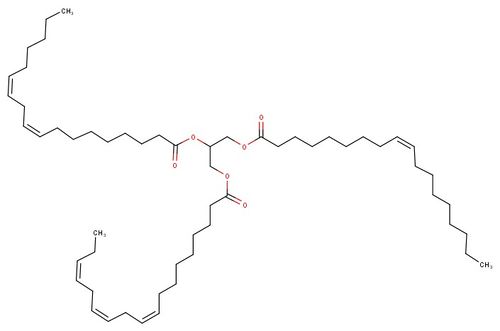
Beim Biodiesel auf Rapsölbasis handelt es sich um ein Stoffgemisch, welches als Rapsölmethyleser (RME) bezeichnet wird. In der oberen Abbildung sind die Strukturformeln einiger Bestandteile dieses Gemisches dargestellt. Darunter findet ihr zum Vergleich die bekannte Struktur eines Rapsöl-Moleküls.
30px Aufgabe 1
Beschreibt den Zusammenhang zwischen den Molekülen im Biodiesel und dem Rapsöl-Molekül. |
Herstellung von Biodiesel
Findet einen geeigneten Reaktionspartner
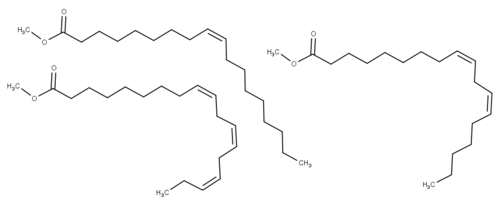
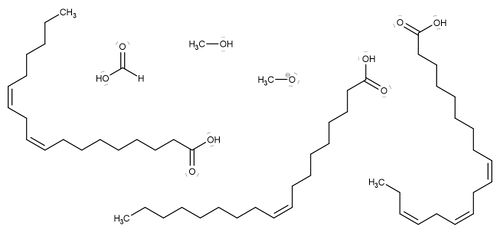
Später sollt ihr aus Rapsöl und einem weiteren Edukt selbst Biodiesel herstellen. Folgende Stoffe stehen als Reaktionspartner zur Auswahl:
30px Aufgabe 2
Wählt aus den abgebildeten Molekülen das aus, welches eurer Meinung nach am besten dazu geeignet ist, mit Rapsöl zu RME umgesetzt zu werden. Begründet eure Entscheidung. |
Habt ihr das richtige Edukt gefunden?
30px Aufgabe 3
Überprüft eure Vermutung aus Aufgabe 2 durch den folgenden Versuch: |
30px Versuch
(in Anlehnung an [1]) Chemikalien: Rapsöl, Edukt aus Aufgabe 2, Salzsäure (0,05 molar) Material: Erlenmeyerkolben (250 mL) mit Stopfen, Becherglas (250 mL), Thermometer, Becherglas (1000 mL), Thermoskanne mit heißem Wasser Durchführung (Abzug! Gefahrensymbole auf dem AB beachten!): Schritt 1: Herstellung des Produkts
Stellt das Kärtchen mit dem Namen eures zweiten Edukts neben den Erlenmeyerkolben und fotografiert es zusammen mit dem Produkt.
Füllt 50 mL Salzsäure in das Becherglas, gebt das Reaktionsgemisch dazu und rührt die Mischung kurz mit dem Glasstab. |
Der Weg zum Biodiesel auf molekularer Ebene
30px Aufgabe 4
Formuliert den Mechanismus für die Reaktion vom Rapsöl mit dem richtigen Reaktionspartner.
Auch bei der Herstellung von RME läuft eine Additions-Eliminierungs-Reaktion ab.
Gesucht wird ein Molekül, welches an einer geeigneten Stelle des Rapsöl-Moleküls besonders gut nucleophil angreifen kann.
Der Mechanismus dieser Umsetzung ist dem ersten Teil des Mechanismus der Verseifung sehr ähnlich.
In dieser LearningApp seht ihr alle Strukturformeln, die für den Mechanismus eine Rolle spielen. Bringt sie in die richtige Reihenfolge. |
- ↑ Ingo Mennerich: Vom Raps zum Biodiesel: Vom Acker in den Tank? Abrufbar unter: http://www.schulbiologiezentrum.info/Arbeitsbl%E4tter%20Raps%20Raps%F6l%20Biodiesel%20Me210212.pdf [01.09.2018]