Thermoplaste: Unterschied zwischen den Versionen
(→PUR) |
(→Quellen) |
||
| Zeile 291: | Zeile 291: | ||
https://www.chemie.de/lexikon/Polyethylen.html | https://www.chemie.de/lexikon/Polyethylen.html | ||
https://www.plasticseurope.org/de/focus-areas/circular-economy/zero-plastics-landfill/recycling-and-energy-recovery | https://www.plasticseurope.org/de/focus-areas/circular-economy/zero-plastics-landfill/recycling-and-energy-recovery | ||
| + | https://www.kunststoffe.de/themen/basics/technische-kunststoffe/polyamide-pa/artikel/polyamide-pa-651963 | ||
| + | https://www.internetchemie.info/chemie-lexikon/funktionelle-gruppen/p/peptid-bindung.php | ||
Version vom 8. November 2018, 20:52 Uhr
Gruppe von Lena, Paulina, Daniel, Alexander, Laura und Lea!
Kaum ein Tag vergeht an dem wir nicht mit Kunststoffen in Kontakt treten. In unserer modernen Welt sind sie ein beliebter Werkstoff welcher vielfältig eingesetzt wird, zum Beispiel in der Fahrzeug- oder der Textilindustrie. Doch Kunststoff ist nicht gleich Kunststoff. Verschiedenste Bedürfnisse brauchen verschiedenste Eigenschaften. Für den Einsatzbereich entscheidend sind Eigenschaften wie Temperaturbeständigkeit, Verformbarkeit und Elastizität. Es ergeben sich die drei Gruppen: Thermoplaste, Duroplaste und Elastomere.
Makromoleküle
Makromoleküle sind meistens Polymere und werden umgangssprachlich auch als „Riesenmolekül“ bezeichnet, da es sich um sehr große Moleküle handelt. Sie bestehen aus sich wiederholenden, gleichen oder unterschiedlichen Atomen oder Atomgruppen, die aus Monomere gebildet werden. Durch ihre Größe hat eine Wegnahme oder Aufnahme von Atomen keinen Einfluss auf die Eigenschaften. Ein Beispiel für ein synthetisches Markromolekül sind zum Beispiel Kunstoffe.
Monomere
Moleküle aus denen Makromoleküle gebildet werden nennt man Monomere. "Monomeres" ist griechisch für einfach und einteilig, was gut die Funktion des Monomers beschreibt, denn es ist die kleinste Einheit welche immer wieder kehrt. Durch Polymerisation, Polykondensation oder Polyaddition reagieren sie zu Polymeren (Makromolekülen). Man unterscheidet zwischen Homopolymeren und Copolymeren, letztere sind Polymeren aus unterschiedlichen Monomeren. Bei Homopolymeren wird ausschließlich eine Monomer-Art benutzt. Benutzt man Aufgebaut sind Monomere meist durch eine C=C Doppelbindung, allerdings sind auch weitere Moleküle denkbar - wichtig sind mindestens zwei funktionelle Gruppen pro Molekül. Ein bekanntes Beispiel ist das Ethen (Ethylen), es wird für Tragetaschen, Eimer und Mülltonnen benutzt.
Thermoplast
Thermoplaste sind Kunststoffe, die bei einer bestimmten Temperatur verformbar sind. Das Wort Thermoplaste lässt sich in zwei Teile aufteilen: "Thermo" steht für Wärme und "Plasten" bedeutet formen. Bei niedrigen Temperaturen sind die Kunststoffe fest. Erwärmt man den Stoff gelangt er zunächst in den thermoelastischen Bereich, indem der Stoff verformbar ist, aber anschließend wieder seine ursprüngliche Form annimmt (bspw. ein Schwamm bei Raumtemperatur) . Wenn man den Kunststoff noch weiter erhitzt, gelangt man in den thermoplastischen Bereich, wo der Stoff ebenfalls verformbar ist, aber im Gegensatz zum anderen Bereich, nicht mehr in seine Ursprungsform zurückgeht. Zuletzt kann man die Kunststoffe so weit erhitzen, bis sie flüssig werden und sich schlussendlich zersetzen. Die Grundstruktur eines Thermoplasts besteht aus mehreren nebeneinander verlaufenden Ketten (Polymeren), welche untereinander nicht vernetzt sind. Diese sind für die thermoplastische Eigenschaft verantwortlich. Somit gilt: Je höher die Temperatur ist, desto besser können die einzeln vorliegenden Polymeren (lineare/strauchähnlich verzweigte Makromoleküle) gegeneinander verschoben werden. Die Verschiebung wiederum ist für die Elastizität notwendig. Man unterscheidet hier zwischen zwei Bereichen. In dem kristallinen Bereich liegen die Ketten geordnet nebeneinander vor und im amorphe Bereiche liegen die einzelnen Ketten ungeordnet und verknäult vor. Je mehr kristalline Bereiche es gibt, desto härter und spröder ist ein Thermoplast.
Zur Veranschaulichung der verschiedenen Bereiche dient dieses Video
Duroplast
Als Duroplast bezeichnet man einen sehr harten, stabilen Kunststoff. Er wird aus Monomeren durch Polykondensation künstlich zusammengesetzt. Durch Atombindungen sind Molekülketten engmaschig 3D verknüpft und daher nur wenig beweglich (Abbildung). Es bestehen mindestens 2-3 Bindungen und somit werden auch mehr als 2 funktionelle Gruppen benötigt. Anders als Thermoplaste sind Duroplaste nicht schmelzbar und nicht durch Lösemittel auflösbar. Bei Hitze zersetzten sie sich lediglich, denn ihre Atombindungen werden gespalten. Allerdings sind Duroplasten, im Gegensatz zu Elastomeren, hart, spröde und können zerbrechen. Aufgrund ihrer Eigenschaften werden sie oft in Computern oder auch Autos verbaut, denn sie sind hitzebeständig, sehr stabil und nicht verformbar.
Elastomer
Die Elastomere gehören zu den Kunststoffen. Sie unterscheiden sich jedoch von den anderen Kunststoffen, wie den Thermoplasten und den Duroplasten besonders durch ihre hohe Elastizität. Daher werden diese Kunstoffe umgangssprachlich auch als „Gummi“ bezeichnet. Ein Beispiel für ein Elastomer wäre somit ein Schwamm oder auch ein Autoreifen. Die Elastomere bestehen aus kleinen organischen Einheiten, diese werden auch als Monomer bezeichnet. Durch Vorgänge wie die Polymerisation, Polyaddition und Polymkondensation werden sie künstlich zusammengeknüpft und liegen anschießend „verknäult“ vor.Eine Besonderheit bei den Elastomeren ist, dass sie durch Kälte spröde werden. Zu einer Zersetzung kommt es jedoch erst ab ca. 300 Grad Celcius. Außerdem lässt es sich durch Druck bzw. Zug verformen, geht anschließend aber wieder in seine Ausgangsform zurück. Dabei speichert es zudem keine Energie. Ein weiteres Merkmal ist die schlechte Löslichkeit der Elastomere, da sie nicht schmelzbar sind und sich auch nicht in Lösungsmittel auflösen. Dies lässt sich auf die Weitmaschige 3D Verknüpfung der Monomere zurückführen.
Recycling
Unter dem Begriff „Recycling“ versteht man die Aufbereitung und Wiederverwendung von Abfällen, aus denen neue Produkte hergestellt werden. Die Abfälle werden dabei zuerst in neue Rohstoffe verwandelt. Es können aber nicht alle Abfälle recycelt werden, denn dies ist nur mit Produkten möglich, die als wiederverwendbare gelten. Gekennzeichnet sind diese durch ein grünes Logo auf dem Produkt. Zudem gibt es drei unterschiedliche Verfahren des Recyclings der Thermoplaste. Diese werden einmal als werkstoffliche Verwertung, rohstoffliche Verwertung und energetische Verwertung bezeichnet. Unter der werkstofflichen Verwertung versteht man die Aufbereitung von bereits verwendeten Kunststoffen, bei der die Struktur unverändert bleibt. Hier werden die einzelnen Teile gereinigt, zerkleinert und letztendlich nach ihren Sorten getrennt. Die rohstoffliche Verwertung beschreibt die Spaltung der Polymerketten. Dies wird beispielsweise durch das Einwirken von Wärme erreicht. Besonderes eignet sich diese Methode für verschmutze, sowie für vermischte Kunststofffraktionen. Die energetische Verwertung beschreibt die Rückgewinnung der Energie, die in den Kunststoffen enthalten ist. Erreicht wird dies durch die Verbrennung der Kunststoffe, wobei die entstehende Energie gleichzeitig für die Stromerzeugung oder ähnliches benutzt wird. Diese Form der Verwertung eignet sich ebenfalls besonders für verschmutze und vermischte Kunstofffraktionen, zusätzlich aber auch für schadstoffbelastete.
Polymerisation
Es gibt verschiedene Möglichkeiten Kunststoffe herzustellen. Man unterscheidet bei den Reaktionsarten zwischen der Polykondensation, der Polyaddition und der Polymereisation. Das verwendete Monomer bestimmt hierbei die Reaktionsart. Die Polymereisation läuft ab wenn mindestens eine C=C Doppelbindung vorliegt. Dies ist entscheidend für den weiteren Verlauf der Reaktion, denn bei dieser brechen Doppelbindungen auf und die verschiedenen Monomermoleküle verbinden sich unter Ausbildung von C-C Einfachbindungen. Liegt nur eine Doppelbindung vor entstehen lange, unverzweigte Ketten. Dieses Verfahren stellt Thermoplasten her.
Polykondensation
Radikale
Radikale sind Atome oder Moleküle, die mindestens ein ungepaartes Valenzelektron besitzen. Valenzelektronen bestimmen die Wertigkeit eines Moleküls und sind für die chemische Bindung verantwortlich. Wegen des ungepaarten Elektrons handelt es sich hierbei um hochreaktive und wenig stabile Moleküle. Deswegen existieren Radikale meist nur sehr kurze Zeit (< 1 Sekunde); eine Ausnahme dabei stellen stabilisierte Radikale dar. Radikale werden mit einem Punkt dargestellt. Ein typisches Merkmal für Radikale ist es, dass sie häufig in Form einer Kettenreaktion reagieren.
Radikalketten-Mechanismus
Startreaktion
Wachstumsreaktion
Abbruchreaktion
Polyester
Polyester sind Polymere mit Esterfunktionen und bilden die große Familie der synthetischen Polymere. Sie werden nach dem Schmelzspinnverfahren hergestellt. Die Polyesterfasern sind widerstandsfähig gegen klimatische Einflüsse und sie die wichtigsten Kunstfasern der Modewelt. Polyestersynthese entsteht durch die ringöffnende Polymerisation, PET und PBT werden durch eine Umesterung hergestellt. Diol wird in der Schmelze am Katalysatorkontakt mit einem Dicarbonsäureester umgesetzt.
Polyurethan
Polyamid
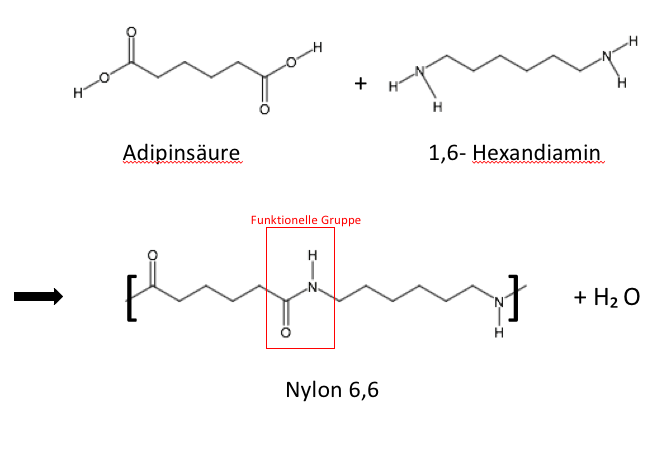
Polyamide zählen zu den wichtigsten technischen Thermoplasten. Sie sind zähe Materialien mit einer hohen Festigkeit und haben eine gute Abriebs- und Verschleißfestigkeit. Außerdem können sie relativ viel Wasser aufnehmen, sind polar und nur gegenüber starken Säuren unbeständig. Die Polyamide ersetzen viele Metallteile im Fahrzeugbau, da sie eine deutlich höhere Wärmeformbeständigkeit und eine gute Beständigkeit gegenüber organischen Lösungsmitteln aufweisen. Außerdem leiten sich fast alle Polyamide von primären Aminen ab. Die funktionelle Gruppe der sich wiederholenden Einheit ist hier (C=O)-(NH).
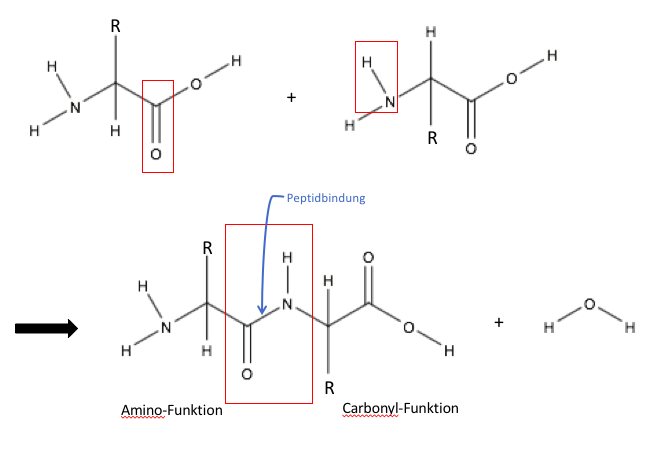
Peptid-Gruppen
Die Peptid-Gruppe ist eine (C=O)-(NH)-Gruppe, welche zwei Aminosäuren miteinander verbindet. Dies ist die Bindung zwischen der Carboxylgruppe einer Aminosäure und der Aminogruppe einer zweiten Aminosäure.
PET
PVC
Herstellung
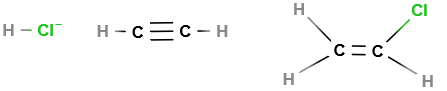
Polyvinylchlorid (PVC) wird durch eine radikalische oder ionische Kettenpolimerisation aus dem Monomer Vinylchlorid (CH² = CHCl) erzeugt. Um es herzustellen, kann man zum einen Ethin und zum anderen Ethen verwenden. Bei der ersten Möglichkeit findet die Reaktion zwischen Chlorwasserstoff(HCl) mit Ethin statt.
Wenn eine Temperatur von 200°C gegeben ist und es unter Druck steht wird Chlorwasserstoff and die Dreifachbindung des Ethins addiert und bildet somit Vinylchlorid. Außerdem muss Quecksilber(II)chlorid als Katalysator vorhanden sein.
Diese Reaktion ist in dem vorliegenden Bild: Herstellung eines Vinylchlorids dargestellt:
| Vinylchloridreaktion | Beschreibung der Reaktion |
|---|---|
|
Am Anfang der Reaktion sind Ethin(H-C=C-H) und Chlorwasserstoff(HCl) vorhanden. Diese werden durch Addition zu Chlorethen(Vinylchlorid). Allerding ist dieses Verfahren veraltet und heutzutage wird Chlor und Ethen addiert wodurch Dichlorethan entsteht, welches mithilfe eines Aluminiumoxid-Katalysators, unter Abspaltung von Chlorwasserstoff(HCl) zu Vinylchlorid umgewandelt wird. Nachdem das giftige Vinylchlorid hergestellt wurde wird es durch Zugabe der Peroxide in der Ketten-Polymerisation zu festem Polyvinylchlorid. Somit erhält man Polyvinylchlorid, wenn man mindestens 2 Monomere Vinylchlorid miteinander polymerisiert. |
Den Verlauf der Polymerisation nochmals allgemeiner erläutert bedeutet, dass es durch eine radikale Polymerisation geschieht, wobei die Aktivierung durch Radikalstarter ,auch Initiatoren genannt, stattfindet. Diese Iniatoren haben schneller eine Kettenreaktion zur Folge als andere Stoffe. In der heutigen Produktion werden bestimmte preisgünstige Peroxide (Initiatoren) , die bereits bei niedrigen Temperaturen wirken, zur Produktion von PVC eingesetzt.
Ein Auschnitt aus dem Aufbau einen Polyvinylchlorids ist in der folgenden Abbildung dargestellt:
Eigenschaften
PVC ist ein harter, spröder, weißer armorpher thermoplastischer Kunststoff. Außerdem würde durch stärkere Erwärmung des PVC, Chlorwasserstoff freigesetzt werden, dies wird durch zum Teil giftige Schwermetallverbindungen, die als Stabilisatoren zugesetzt werden, verhindert. Ebendso wird es beim Erhitzen weich und plastisch verformbar, wie bei den meisten Thermoplasten. PVC ist geruchs- und geschmachsfrei, beständig gegen Wasser, gegen viele organische Lösungsmittel und gegen schwache Säuren und Basen. Nachteil ist, dass es eine schlechte elektrische Leitfähigkeit besitzt und sich bei Wärmeeinwirkung langsam zersetzt. Die Dichte beträgt 1,38 und die Druckfestigkeit 55- 90 MPa. Zudem ist es schwer entflammbar.
| PVC | Dichte | Druckfestigkeit | Hitze | Sinneseindrücke | Beständigkeit gegen | Sonstiges |
|---|---|---|---|---|---|---|
| PVC | 1,38 | 55-90 MPa | Schwer entflammbar, wird weich und verformbar | Ist geruchs und geschmackslos | Wasser, organische Lösungsmittel, schwache Säuren/Basen | Schlechte elektische Leitfähigkeit und langsame Wärmeeinwirkung |
Anwendung
PVC wird seit 1913 technisch hergestellt, aber wurde erst in den 50er Jahren zu einem der wichtigsten Kunststoffe des täglichen Gebrauchs. PVC ist sehr vielseitig einsetzbar, das sogenannte Hart-PVC wird für Haushaltsgegenstände, Verpackungsmaterial, Platten, Rohre, Ventile und Hähne verwendet. Wenn man Weichmacher, z.B. Phthalsäureester in Verbindung mit PVC verwendet entsteht Weich-PVC welches zur Herstellung von Schläuchen und Fußbodenbelägen oder Kunstleder verwendet wird.
Probleme
Im Laufe der Zeit wurde PVC immer weiter verbreitet eingesetzt, allerdings ist PVC durch das Vinylchlorid giftig und Arbeiter, die mit PVC-Produktion in Verbindung standen, wurden krank und anschließend wurde die VC(Vinylchlorid-Krankheit) als Berufskrankheit anerkannt. Außerdem könnten Weichmacher entweichen, wenn PVC als Babyspielzeug verwendet wird und die Babys daran lutschen, daher wurde es für diesen Zweck in Deutschland verboten. Ebendso schlecht steht es für die Entsorgung von PVC, da die Entsorgung ein teurer Prozess ist, der einen Einbau einer Abgasreinigung in Verbrennungsanlagen zur Folge hätte.
PUR
Herstellung
Theorie
Polyurethan(PUR) entsteht durch die Polyadditionsreaktion von Polyisocyanaten mit Polyolen. Diese Verknüpfung entsteht durch die Reaktion einer Isocyanatgruppe(-N=C=O) eines Moleküls mit einer Hydroxylgruppe (-OH) eines anderen Moleküls unter Bildung einer Urethangruppe(-NH-CO-O-). Allerdings erfolgen mit der Abspaltung keine Nebenprodukte wie bei der Polykondensation. Die Polyurethanbildung erfordert mindestens zwei verschiedene Monomere, am einfachsten ist es mit Diol und Diisocyanat. Die Bildung ensteht in Stufen. Zuerst entsteht aus Diol und Diisocyanat ein bifunktionelles Molekül mit einer Isocyanatgruppe(-N=C=O) und einer Hydroxylgruppe(-OH).
Praxis
In der Praxis gibt es zwei mögliche Wege:
- Die direkte Reaktion eines Polyols mit einem Polyisocyanat(ein Einstufen-Verfahren)
- Herstellen eines funktionalisierten kleineren Polymers(sogenanntes Prepolymer) als Zwischenprodukt, was im zweiten Schritt durch Verlinken der funktionellen Gruppe zum gewünschten Polymer reagiert(ein Zweistufen-Verfahren
Eigenschaften
Je nach Wahl des Isocyanats und des Polyols kann ein Polyurethan unterschiedliche Eigenschaften aufweisen. Allerdings liegt die Dichte von ungeschäumten PUR zwischen rund 1000 und 1250 kg/m³. Meistens werden diese Eigenschaften mithilfe der Veränderung der Polyolkomponente verändert, da diese öfter chemisch eingesetzt. Somit gibt es verschiedene Formen des Polyurethans die im folgenden aufgelistet sind:
- Diphenylmethandiisocyanat (MDI)
- Polymeres Diphenylmethandiisocyanat (PMDI)
- Toluylendiisocyanat (TDI)
- Naphtylendiisocyanat (NDI)
- Hexamethylendiisocyanat (HDI)
- Isophorondiisocyanat (IPDI)
Wenn Polyurethane ausreagiert sind und keine Monomere mehr enthalten, sind sie in der Regel nicht mehr gesundheitsschädlich, allerdings können Isocyanate Allergien auslösen und stehen im Verdacht Krebs zu verursachen.
Anwendung
Polyurethan wird meisten als Füllstoff für die verschiedstens verwendet, da es eine Schaumartige Struktur hat. Aus PUR werden Matratzen, Schuhsohlen, Dichtungen, Schläuche, Fußböden, Lacke, Klebstoffe, Dichtstoffe, Skier, Autositze, Laufbahnen in Stadien, Armatirenbretter, Vergussmassen, Kondome(Präservative) und vieles mehr hergestellt. Ebendso wird bei der Herstellung von modernen Fußbällen Polyurethan als Füllstoff verwendet,auch der äußerste Mantel einer Bowlingkugel besteht aus PUR und noch in vielen anderen Bereichen wird PUR eingesetzt.
PE
Herstellung
Polyethylen (PE) wird durch die Polymerisation von Ethen hergestellt. Daher hat es die vereinfachte Strukturformel (-H2C-CH2-). Je nach Druck entstehen verschiedene Arten des Polyethylen: Beim Hochdruckverfahren das Weich-Polyethylen (PE-LD), im Niederdruckverfahren das Hart-Polyethylen (PE-HD). Bei beiden Verfahren ist das Polyethylen zunächst eine zähe Flüssigkeit, allerdings werden im Niederdruckverfahren geträgerte Katalysatoren eingesetzt und somit fällt das Polyethylen in Form fester Körner an.
Eigenschaften
- niedrige Dichte(0,87-0,965 g/cm³)
- hohe Zähigkeit und Reißdehnung
- positives Gleitverhalten, geringer Verschleiß
- optisch milchig weiß
- sehr gutes elektrische und dielektrisches Verhalten
- geringe Wasseraufnahme
Anwendung
- PE-LD und PE-LLD werden vorallem in der Folienproduktion eingesetzt => Müllsäcke,Schrumpffolien und Landwirtschaftsfolien werden damit hergestellt
- PE-HD wird vorallem zum herstellen von Hohlkörper benutzt => Flaschen für Haushaltsreinigungsmittel und auch großvolumige Behälter mit bis zu 1000 l. Außerdem wird es für Wasserbau- und Deponiebaufolien verwendet. Ein weiteres großes Einsatzgebiet ist die Gas- und Trinkwasserversorgung
- PE-UHMW wird für Pumpenteile, Zahnräder, Gleitbuchsen, Implantate und Oberflächen von Endoprothesen verwendet. PE-UHMW gehört zu einem der stärksten bekannten künstlichen Fasern, welches als Material für einen Weltraumlift im Gespräch sind
Hydrolyse
Pyrolyse
Bei der Pyrolyse werden Thermoplasten in ihre Polymere durch Hitze einwirkung zerlegt
Recycling-Code
energetische Verwendung
Quellen
https://de.wikipedia.org/wiki/Monomer Chemie Buch: elemente chemie 2 (Seite 306 ff.) https://www.lernhelfer.de/schuelerlexikon/chemie-abitur/artikel/polyvinylchlorid-pvc https://www.chemie.de/lexikon/Polyethylen.html https://www.plasticseurope.org/de/focus-areas/circular-economy/zero-plastics-landfill/recycling-and-energy-recovery https://www.kunststoffe.de/themen/basics/technische-kunststoffe/polyamide-pa/artikel/polyamide-pa-651963 https://www.internetchemie.info/chemie-lexikon/funktionelle-gruppen/p/peptid-bindung.php