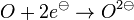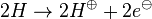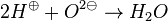Muss Wasser eine Ionenverbindung sein?
Wir haben uns zuletzt sehr intensiv mit Verbindungen beschäftigt, die aus Ionen bestehen. Die Bildung von Ionen, also die Übergabe von Elektronen, die bei Reaktionen von bestimmten Stoffe miteinander stattfindet, hat uns die Möglichkeit gegen, zu erklären, was bei einer chemischen Reaktion wirklich passiert. Denn davor waren chemischen Reaktionen nur Phänomene und Beobachtungen, die wir von außen machen konnten. All dies war möglich, weil wir uns mit dem Atombau beschäftigt haben und das Bestreben der Atome erkannten, den Edelgaszustand durch die Veränderung der Elektronenanzahl zu erreichen. Nebenbei, war die Existenz von Ionen auf eine Möglichkeit die typischen Eigenschaften von Ionenverbindungen zu erklären.
Man kann nun den Eindruck haben, dass alles um uns herum aus Ionen aufgebaut sein müsste! Oder gibt es andere eine andere Möglichkeit, den Edelgaszustand zu erreichen?
Betrachten wir dazu einmal einen sehr alltäglichen Stoff, das Wasser.
Die Formel des Wassers ist bekannt: H2O. Nehmen wir mal an, Wasser wäre eine Ionenverbindung. Dann müsste ja bei der Reaktion von zwei Wasserstoff-Atomen mit einem Sauerstoff-Atom folgendes stattfinden:
1.) Bildung der Ionen
- Durch die Aufnahme der zwei Elektronen erreicht das Sauerstoff-Atom den Edelgaszustand. Damit dies möglich ist, braucht es also Elektronen vom Wasserstoff. Die Wasserstoffatome geben damit ihre einzigen Elektronen ab und somit haben sie keine Schale mehr. Damit hat man eigentlich keinen Edelgaszustand, aber zumindest eine leere äußerste Schale.
2-) Gitterbildung
- Damit hätte man also eine Ionenverbindung mit der Formel H2O.
Rein theoretisch scheint es also durchaus möglich zu sein, dass Wasser eine Ionenverbindung ist. Wenn man sich allerdings daran erinnert, dass die Ionen ja auch die Eigenschaften des Stoffes bestimmen, so stellen sich doch Widersprüche ein, wenn man die typischen Eigenschaften von Ionenverbindungen mit denen von Wasser vergleicht.
So haben Ionenverbindungen typischerweise hohe Schmelz- und Siedetemperaturen. Dazu ein Vergleich:
- Siedetemperatur von H2O: 100 °C
- Siedetemperatur von NaCl: 1465 °C
Schmelzen von Salzen sind auch Stromleitfähig, was bei reinem Wasser nicht der Fall ist. Fasst man dies alles zusammen, muss man zu dem Ergebnis kommen:
| Aufgrund seiner Eigenschaften, wie den sehr niedrigen Schmelz- und Siedetemperaturen und weil es nicht stromleitfähig ist, kann Wasser keine Ionenverbindung sein. Damit müsste eine eine andere Möglichkeit für Atome geben, den Edelgaszustand zu erreichen, als Ionen zu bilden. |
Edelgaszustand durch Überlagerung der Schalen
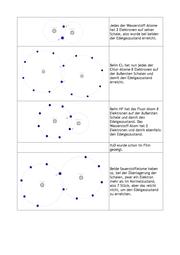
Betrachte dir diesen kleinen Film, um zu sehen, wie man beim Wasser den Edelgaszustand erreichen kann, ohne Ionen zu bilden.
Damit haben wir eine Lösung für das Problem gefunden. Die Wasserstoff- und das Sauerstoffatom überlagern ihre Schalen. Dabei stellt jeweils einer der Bindungspartner dem anderen ein Elektron zur Mitbenutzung zur Verfügung. Sie benutzen jeweils ein Elektron des anderen Atoms gemeinsamen. So erreichen alle drei Atome ihren Edelgaszustand ohne das ein Elektron abgegeben werden muss, wodurch ja Ionen entstehen würden. Das entstandene Produkt hat keine Ionenladung und damit ist zu erklären, dass die Eigenschaften des Wasser nicht denen einer Ionenverbindung gleichen.
| Durch Überlagerung der Schalen können Atome ein Teil ihrer Elektronen gemeinsam benutzen. Dadurch wird der Edelgaszustand erreicht, ohne das Ionen gebildet werden. |
|
Versuche ähnlich, wie im gezeigten Beispiel den Edelgaszustand durch Überlagerung der Schalen zu erreichen. Die Atome können am Kern angefasst und verschoben werden. Die Drehung ist möglich, wenn man das blaue Elektron anfasst, das mit e- beschriftet ist.
|