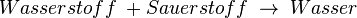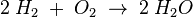Anwendung der Symbolschreibweise 2 - Reaktionen beschreiben
|
Nachweis zur selbstständigen Erarbeitung des Themas Reaktionen mit der Symbolschreibweise beschreiben |
Inhaltsverzeichnis |
Warum bringt die Symbolschreibweise mehr als Worte ?
Bisher haben wir die Edukte und Produkt einer chemischen Reaktion immer mit Worten beschrieben. Lästig ist daran vor allem, dass die Namen manchmal etwas lang sind. Einige von euch waren deshalb versucht, die Symbolschreibweise, die ihr das erste Mal schon vor einiger Zeit kennengelernt hattet, beim Aufschreiben von Reaktionen zu nutzen.
Allerdings ist dies nicht so einfach, denn beim Reaktionsschema wird die Reaktion nur qualtitativ betrachtet:
Es geht also nur darum, welche Stoffe an der Reaktion beteiligt sind.
Eine Reaktionsgleichung dagegen enthält sowohl qualtitative als auch quantitative Informationen:
Hier wird nämlich genau angegeben wieviele Wasserstoff- und Sauerstoffatome da miteinander reagieren und wieviele Wassermoleküle dabei heraus kommen. Man muss dann nämlich auch dabei beachten, dass die Anzahl der Wasserstoffatome, die man in die Reaktion "hineinsteckt" auch hinten wieder "hinauskommen". Denn Atome können weder zerstört noch plötzlich erschaffen werden.
Der Vorteil ist, das man etwa hier in dem Beispiel schon vorhersagen kann, wieviel Sauerstoff ich brauche, damit ich ein Stöchiometrisches Knallgas-Gemisch habe. Ich habt ja schon mitbekommen, das die Reaktion von reinem Wasserstoff mit der Umgebungsluft sehr viel schwächer ist, als wenn man es mischt.
Begleitet wird und dabei das Eisen ... wie im Bild oben angedeutet ... an dem wir exemplarisch Reaktionen in Symbolschreibweise notieren und später auch quantitative Berechnungen vornehmen werden. Bei den Eisenoxiden haben wir auch die Besonderheit, die wir schon von anderen Metallen kennen. Dass es nämlich verschiedene Oxide gibt, bei denen das Atomanzahlverhältnis von Eisen- zu Sauerstoff-Atomen unterschiedlich ist. Mit der Symbolschreibweise können wir das aber ganze genau angeben.