Übungen zum Redoxbegriff: Unterschied zwischen den Versionen
(+ 7 categories using HotCat) |
|||
| Zeile 41: | Zeile 41: | ||
{{Kurzregel|Folgende Regeln sollte man beachten: | {{Kurzregel|Folgende Regeln sollte man beachten: | ||
* Die Atome der Hauptgruppen-Elemente versuchen den Edelgaszustand (meist 8 Außenelektronen) zu erreichen, indem sie Elektronen aufnehmen oder abgeben. Z.B.Na erreicht Ne-Elektronenkonfiguration und P erreicht Elektronenkonfiguration von Ar. <small>''Die Ausnahme ist das Helium mit zwei Außenelektronen''</small> | * Die Atome der Hauptgruppen-Elemente versuchen den Edelgaszustand (meist 8 Außenelektronen) zu erreichen, indem sie Elektronen aufnehmen oder abgeben. Z.B.Na erreicht Ne-Elektronenkonfiguration und P erreicht Elektronenkonfiguration von Ar. <small>''Die Ausnahme ist das Helium mit zwei Außenelektronen''</small> | ||
| − | * Da der Edelgaszustand immer durch Abgabe <u>oder</u> Aufnahme erreicht werden kann, wird es meist so sein, das so wenig wie möglich Elektronen aufgenommen oder abgegeben werden. Also <math>As | + | * Da der Edelgaszustand immer durch Abgabe <u>oder</u> Aufnahme erreicht werden kann, wird es meist so sein, das so wenig wie möglich Elektronen aufgenommen oder abgegeben werden. |
| + | ::Also <math>As + 3 e^{ \ominus}\rightarrow As^{ 3 \ominus}</math> statt <math>As \rightarrow As^{ 5 \oplus} + 5 e^{ \ominus}</math>. | ||
* Die <u>Gesamt</u>anzahl an aufgenommenen oder abgegebenen Elektronen soll so klein wie möglich sein, wenn man eine Ionen-Verbindung betrachtet. | * Die <u>Gesamt</u>anzahl an aufgenommenen oder abgegebenen Elektronen soll so klein wie möglich sein, wenn man eine Ionen-Verbindung betrachtet. | ||
* In Ionenverbindungen haben Metalle meist eine positive Ladung, die Nichtmetalle haben meist eine negative Ladung und die {{wpde|Halbmetalle|Halbmetalle}} haben je nach Partner eine positive oder negative Ladung. <small>''Diese Regel kann aber nicht für Moleküle verwendet werden, dabei wird die Oxidationszahl mit eigenen Regeln bestimmt!''</small> | * In Ionenverbindungen haben Metalle meist eine positive Ladung, die Nichtmetalle haben meist eine negative Ladung und die {{wpde|Halbmetalle|Halbmetalle}} haben je nach Partner eine positive oder negative Ladung. <small>''Diese Regel kann aber nicht für Moleküle verwendet werden, dabei wird die Oxidationszahl mit eigenen Regeln bestimmt!''</small> | ||
Version vom 30. März 2017, 10:04 Uhr
Die Sammlung der folgenden Aufgaben ist sehr ausführlich und es werden teilweise Aufgaben gestellt, die für bessere Schüler langweilig erscheinen. Wenn du weißt, dass du nicht so stark bist, bearbeite alle Aufgaben nacheinander. Nur wenn du dir sicher bist, dass du eine Aufgabe kannst, solltest du sie überspringen. Teilweise kann man ja die ersten Aufgaben schon bearbeiten und die dann kontrollieren. Wenn alles richtig ist, überspringe die Aufgaben, die dir zu leicht erscheinen.
Hier nun noch mal die wichtigen Begriffe ...
Zur Erinnerung:
|
Unter einem Redoxpaar versteht man ein Paar von Teilchen, die durch Auf- bzw. Abnahme ineinander überführt werden können.Zum Beispiel:
|
|
|
Eine Grundlegende Aufgabe ist die Bestimmung der Ladung von Ionen der Hauptgruppenelemente. Weil diese Aufgabe so grundlegend ist, wird sie für einige etwas einfach sein, aber Übung schadet trotzdem ist, oder? Das PSE ist hier ein wichtiges Hilfsmittel!
Folgende Regeln sollte man beachten:
|
|
|
|
|
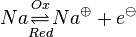 und
und 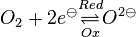
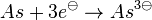 statt
statt 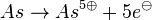 .
.

