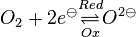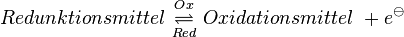Gewinnung von Brom am Toten Meer: Unterschied zwischen den Versionen
(→Redoxreaktionen am Beispiel der Bromgewinnung) |
(→Redoxreaktionen am Beispiel der Bromgewinnung) |
||
| Zeile 139: | Zeile 139: | ||
:<math>Na \underset{Red} {\overset{Ox} \rightleftharpoons} Na ^{ \oplus} + e^{ \ominus}</math> und <math>O_2 + 2 e^{ \ominus} \underset{Ox} {\overset{Red} \rightleftharpoons} O ^{2 \ominus} </math> | :<math>Na \underset{Red} {\overset{Ox} \rightleftharpoons} Na ^{ \oplus} + e^{ \ominus}</math> und <math>O_2 + 2 e^{ \ominus} \underset{Ox} {\overset{Red} \rightleftharpoons} O ^{2 \ominus} </math> | ||
Allgemein kann man es so formulieren ''(wobei Ladungen der Ionen nicht angegeben sind)'': | Allgemein kann man es so formulieren ''(wobei Ladungen der Ionen nicht angegeben sind)'': | ||
| − | :<math>Red \ \rightleftharpoons \ | + | :<math>Redunktionsmittel \ \underset{Red} {\overset{Ox} \rightleftharpoons} \ Oxidationsmittel \ + e^{ \ominus}</math> |
}} | }} | ||
Version vom 10. März 2016, 03:38 Uhr
Inhaltsverzeichnis |
Warum Brom?
Über einer dunklen, rotbraunen Flüssigkeit wabert ein schwerer rotbrauner Dampf, der sich im Raum verteilt. Seinen Namen verdankt Brom dem griechischen Begriff für Gestank (= brômos), den Brom zurecht hat, denn Bromdampf hat einen intensiven, chlorähnliches Geruch, den man schon in kleinsten Mengen wahrnehmen kann. Den sollte man sich aber nicht zu häufig antun, denn Brom ist giftiger als Chlor. Deshalb ist Elementares Brom in den Schulen verboten, zumal eine umgeworfene und ausgekippte Flasche Brom meist zur Evakuierung der gesamte Schule führt (Feuerwehr-Bericht als Beispiel)
Trotz seiner unangenehmen Eigenschaften gibt es zahlreiche Einsatzgebiete für das "Teufelszeug", von denen hier nur eine kleine Auswahl genannt wird. Eine ausführlichere und genauer Liste liefert der Wikipedia-Artikel 19px Brom :
- es gibt organische Bromverbindungen die als Flammschutzmittel dienen
- früher gab es zahlreiche Medikamente, die Brom bzw. Bromide enthielten, heute gibt es besseren Ersatz
- für die Fotoindustrie wird Silberbromid als lichtempfindliche Suspension verwendet, die auf Fotoplatten verwendet wird
- im Labor dient es zum Nachweis von Doppel- und Dreifachbindungen
- Bromlösungen können als mildes Desinfektionsmittel verwendet werden (milder als Chlor)
Anhand des Broms werden wir einige Themen aus der Mittelstufe wieder aufgreifen und vertiefen und damit erklären, woher die Eigenschaften von Brom und Bromverbindungen kommen, um diese dann auf die anderen Halogene übertragen zu können.
Gewinnung von Brom am Toten Meer
Das Tote Meer ist ein abflussloser See, dessen Wasseroberfläche etwa 428 m unter dem Meeresspiegel liegt. Die Entstehung dieses tiefen, schmalen und langen Landstreifens, der als "syrisch-afrikanischen Riss" bezeichnet wird, lässt sich dadurch erklären, das dieses Gebiet in der Erdkruste abgesunken ist. Dies geschah allerdings geschätzt vor mehreren Hundert-Millionen Jahren. Das Tote Meer wird vom Jordan gespeist und ist für seinen hohen Salzgehalt bekannt Er grenzt an Jordanien, Israel und das von Israel besetzte Westjordanland.
Das besondere am Toten Meer ist der Salzgehalt von bis zu 33 %, im Durchschnitt ist er bei etwa 28 %. Zum Vergleich dazu ist der Salzgehalt des Mittelmeeres mit nur etwa 3,8 % wesentlich geringer. Aufgrund des hohen Salzgehalts hat das Seewasser eine Dichte von ca. 1,240 kg/l.
Diese hohe Salzkonzentration ist dadurch entstanden, das es durch den Zufluss von Wasser aus dem Jordan und aufgrund des trockenen Wüstenklima stetig verdunstenden Wassers, zu einer Anreicherung von Mineralien und Salzen kommt. Der Zufluss von Jordanwasser und den Entzug von Verdunstungswasser haben sich mit der Zeit auf die Höhe des aktuellen Wasserspiegels eingependelt. Negativ beeinflusst wird der Wasserpegel durch die künstliche Verdunstung der kommerziellen Salzgewinnung.
- PikiWiki Israel 32639 Ein Feshkha.JPG
Blick von 19px Ain_Feshkha im Westjordanland auf das Tote Meer.
- Dead sea newspaper.jpg
Aufgrund der hohen Dichte, kann man sich ins Wasser legen und bequem lesen.
- Dead Sea Halite View 031712.jpg
Ausgedehnte Salzkrusten am Strand.
Entgegen dem Namen ist das Tote Meer übrigens biologisch nicht tot, jedoch beschränkt sich das Leben weitgehend auf verschiedene Lebewesen und Pflanzen, die an die extremen Bedingungen angepasst sind. Es gibt vor allem halophile (=salzliebende) Mikroorganismen, wie zum Beispiel anaerobe (=Leben ohne Sauerstoff) Bakterien die zum Beispiel Salpeter, Schwefel und Cellulose abbauen. Auch manche Pflanzen mit großer Salztoleranz können in dieser extremen Umwelt überleben.
Warum die Brom-Gewinnung am Toten Meer?
Die größten Brom-Produzenten sind die Vereinigten Staaten, China, Israel, sowie Jordanien. Nach den zwei Riesenindustriestaaten kommen die zwei der Anrainer des Totes Meeres. In sofern scheint es klar zu sein, dass es da Zusammenhang geben muss. Neben der hohen Salzkonzentration gibt es nämlich auch noch deutliche Unterschiede bei der Zusammensetzung des Salzes des Toten Meeres im Vergleich zu normalem Meerwasser.
| Bestandteil | Anteil in Prozent im trockenen Salz | Mengen im Wasser des Toten Meer |
|---|---|---|
| MgCl2 | 50 % | 22 Mill. t |
| NaCl | 30 % | 12,5 Mill. t |
| CaCl2 | 14 % | 6 Mill. t |
| KCl (Pottasche) | 4 % | 2 Mill. t |
| MgBr2 | 2% | 1 Mill. t |
| CaSO4(Gips) | 0,2 % | 0,215 Mill. t |
Scheinbar nicht sonderlich hoch aber dennoch bemerkenswert ist dabei vor allem das Verhältnis von Chlorid- zu Bromid-Ionen. Im Mittelmeer beträgt das Verhältnis von Chlorid- zu Bromid-Ionen 280 : 1, dagegen ist das Verhältnis im Wasser des Toten Meeres 40 : 1. Damit ist das Tote Meer das Gewässer mit dem höchsten Bromid-Gehalt weltweit.
| Zur Erinnerung: Die einfach negativ geladenen Ionen der Elemente der 7. Hauptgruppe nennt man entsprechend des Gruppennamens allgemein Halogenid-Ion, entsprechend ist F⊖ Fluorid-Ion, Cl⊖ Chlorid-Ion, Br⊖ Bromid-Ion und I⊖ Iodid-Ion. |
Was die Gewinnung am Toten Meer sinnvoll und vor allem wirtschaftlich macht, ist das in der Gegend vorherrschende Klima. Am Toten Meer ist es ganzjährig sonnig bei gleichzeitig geringer Luftfeuchtigkeit und stetigem leichten Wind. Im Jahresverlauf fallen weniger als 50 mm Niederschlag. Die Höchsttemperaturen bewegen sich im Sommer zwischen 32 und 39 °C, im Winter zwischen 20 und 23 °C. Überr die Hälfte des Jahres ist die Tageshöchsttemperatur über 30 °C.
Diese Bedingungen ermöglichen eine Anreicherung des Salzwasser in großen Verdunstungsbecken am südlichen Ende des Toten Meeres. Nachdem einige Bestandteile - vor allem MgCl und NaCl - zum Teil ausgefallen sind, erreicht die Konzentration 10-12 g/l, bei einem Verhältnis von Chlorid- zu Bromid-Ionen 17 : 1.
| Ausfällen: Durch Verdunstung, und damit Veringerung, des Lösungmittels erhöht sich die Konzentration des Salzes immer mehr. Irgendwann reicht die Menge des Lösungsmittels nicht mehr aus, um das gelöste Salz in Lösung zu halten. Es fällt aus, d.h. es bildet sich am Boden ein fester Bodensatz von nicht mehr löslichem Salz. |
Auf Israelischer Seite wird das Brom seit etwa 1900 industriell in der Dead Sea Bromine Company, hergestellt, die ein Bestandteil der israelischen staatlichen Firma Deas Sea Works ist. Neben Brom stellt die Dead Sea Works auch Magnesiumchlorid, Industriesalz, Flugzeugenteisungsmittel, Badesalz, Tafelsalz sowie Rohmaterial für die Kosmetikindustrie her. Weltweit ist die Gesellschaft an vierter Stelle beim Abbau von Kaliprodukten.
Der Prozeß zur Gewinnung von Brom
Hinter der Gewinnung von Brom aus einer Bromid-Lösund steckt im wesentlichen die Reaktion, die im folgenden Film gezeigt wird. Es wäre ratsam, den Film schon bei 38 Sek. zu beenden, um sich von den folgenden, sehr ähnlichen Experimenten, nicht ablenken zu lassen.
Die Rotfärbung der Flüssigkeit zeigt, dass Brom entstanden ist, das sich gleich im Wasser gelöst hat. Im Labormaßstab geht die Gewinnung von elementaren Brom also recht einfach, indem man Chlorgas in die Bromidsalzlösung einleitet. Damit sich der Aufwand für eine industrielle Gewinnung - auch unter Beachtung der Sicherheitsmaßnahmen - lohnt, musste ein Verfahren entwickelt werden, in dem kontinuierlich und ohne Unterbrechung der Produktionsprozess stattfinden kann. Das folgende Bild zeigt den Ablauf mit seinen einzelnen Stationen.
Das Wasser aus dem Toten Meer wird in den Verdunstungsbecken konzentriert, wobei von der sehr viel größeren Menge der Chloridverbindungen ein Teil ausfällt. Dadurch wird der Anteil an Bromid-Ionen erhöht. Diese Lösung wird in die Produktionsanlage geleitet, wo in größeren Behältern die Lösung von heißem Dampf und Chlorgas durchströmt wird. Das Chlor reagiert mit den Bromid-Ionen und es entsteht Brom. Das noch enthaltene, gelöste Salz mit Chlorid-Ionen stört diesen Vorgang nicht und bleibt unverändert.
Durch die Wärme des Dampfes verdunstet das Brom und wird zusammen mit nicht reagiertem Chlor abgeleitet. In einem Kühler wird das Brom, Chlor und auch auch verdunstetes Wasser kondensiert. Das Wasser kann abgetrennt werden, da flüssiges Brom sich nicht mit Wasser mischt und sich aufgrund der höheren Dichte unten absetzt. Um das nun vor allem noch mit Chlor versetzte Brom zu reinigen wird es destilliert und wieder so kondensiert, dass kein Chlor mehr enthalten ist. Das immer noch mit Bromresten verunreinigte restliche Chlorgas kann wieder in den Reaktionsbehälter zurückgeleitet werden, ergänzt um neues Chlor.
Abschließend wird das Brom noch von restlichem Wasser gereinigt, indem hochkonzentrierte Schwefelsäure hinzugefügt wird, dass das Wasser aufnimmt und dann als verdünne Schwefelsäure wieder abgeleitet wird. Das nun reine Brom wird abgeleitet und abtransportiert werden.
Die Ausbeute in der Produktion kann verbessert werden, wenn das meist etwas alkalische Meerwasser mit Hilfe von Schwefelsäure angesäuert wird. Ansonsten würden elementares Brom und Chlor mit dem Wasser reagieren und zunächst Bromwasserstoff bzw. Chlorwasserstoff (=Salzsäuregas) bilden, die den pH-Wert neutralisieren. Dabei wird aber auch die Ausbeute an Brom verringert.
Redoxreaktionen am Beispiel der Bromgewinnung
Im Text des letzten Abschnitts wird nicht nur der technische Ablauf beschrieben, sondern auch welche Stoffe bei der Reaktion beteiligt sind. Den chemischen Vorgang werden wir uns nun genauer anschauen.
30px Aufgabe 1
Beantworte die folgenden Fragen, um zu testen, ob du verstanden hast, was chemisch dabei passiert. |
30px Aufgabe 2
Halte die Reaktion, die bei der Gewinnung von Brom stattfindet fest und bestimme die Oxidation und Reduktion, sowie das Oxidations- und das Reduktionsmittel. |
Zur Erinnerung:
|
Unter einem Redoxpaar versteht man ein paar von Teilchen, die durch Auf- bzw. Abnahme ineinander überführt werden können.Zum Beispiel:
Allgemein kann man es so formulieren (wobei Ladungen der Ionen nicht angegeben sind): |
30px Aufgabe 3
Auf einer Unterseite gibt es eine größere Sammlung von Aufgaben, bei denen du die Anwendung der Begriffe ausführlich üben kannst. → Übungen zum Redoxbegriff |
Bestimmung der Oxidationszahl
Eigenschaften von Brom und den anderen Halogenen
Um zu verstehen, wie die Bromgewinnung funktioniert und warum sich Halogene und ihre Verbindungen so verhalten, schauen wir uns die Hauptgruppe der Halogene noch einmal genauer an.
???
Quellen im Internet
- Das Brom-Buch (auf englisch) wurde vom Israelischen Weizmann Institut of Science und der schon erwähnten Dead Sea Bromine Group herausgegeben. In mehreren Kapiteln bekommt man wirklich sehr ausführliche Informationen zu Brom, dessen Gewinnung und Verwendung.
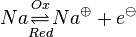 und
und