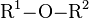Aktuelle Forschung zu neuen Treibstoffen: Unterschied zwischen den Versionen
Aus Chemie digital
(→Benennung Ether) |
(→Ether) |
||
| Zeile 16: | Zeile 16: | ||
== Ether == | == Ether == | ||
| − | |||
| − | |||
[[Datei:Ether.png|mini|Struktur und Bindungsverhältnisse der Ether]] | [[Datei:Ether.png|mini|Struktur und Bindungsverhältnisse der Ether]] | ||
Allgemein kann ein Ether als | Allgemein kann ein Ether als | ||
| Zeile 23: | Zeile 21: | ||
:<math>\mathrm{R^{1}{-}O{-}R^{2} \ }</math> | :<math>\mathrm{R^{1}{-}O{-}R^{2} \ }</math> | ||
| − | dargestellt werden. R<sup>1</sup> und R<sup>2</sup> sind hier Alkyl-Reste. Die Bindungsverhältnisse in Ethern ähneln denen in | + | dargestellt werden. R<sup>1</sup> und R<sup>2</sup> sind hier Alkyl-Reste. Die Bindungsverhältnisse in Ethern ähneln denen in Alkoholen und im Wasser, das als Grundkörper dieser beiden Verbindungsklassen aufgefasst werden kann. Mit den zwei freien Elektronenpaaren am Sauerstoff führt es zu einer tetraedrischen Anordnung der vier Elektronenwolken bzw. zu einem Winkel am Sauerstoff. Der Bindungswinkel des Sauerstoffs ist aufgrund der gegenüber Wasserstoff (104,5° im H<sub>2</sub>O) voluminöseren Alkylsubstituenten mit 112° erweitert. |
| − | + | === Benennung Ether === | |
| − | * Die Verbindung H<sub>3</sub>C–O–CH<sub>3</sub> setzt sich zusammen aus einem H<sub>3</sub>C–O-Substituenten und dem Methyl-Rest (CH<sub>3</sub>) als Stamm, wobei hier allerdings beide Reste gleichwertig sind. Entsprechend heißt die Verbindung Methoxymethan oder | + | Gemäß der IUPAC-Nomenklatur werden aliphatische Ether als Alkoxy-Alkane bezeichnet: R<sub>1</sub>–O–R<sub>2</sub> |
| + | * Die die Gruppe O–R<sub>2</sub> ist ein Alkoxy-Substituent einer Alkan-Kette R<sub>1</sub> behandelt wird. | ||
| + | * Der niederrangigere Substituent der Kette ist hierbei der Alkoxy-Rest (–O–R<sub>2</sub>), der höherrangigere bildet den Stamm des Stoffnamens. | ||
| + | * Ebenfalls von der IUPAC zugelassene Namen werden durch Nennung der beiden Alkylreste und der Endung '''ether''' gebildet und sind besonders für kleine, aliphatische Ether gebräuchlich. | ||
| + | * Bei symmetrischen Ethern ist dann die Bezeichnung sehr einfach durch Vorstellen eines Di möglich [z. B.: Diethylether (Ethoxyethan) oder Dimethylether (Methoxymethan)]. Cyclische und aromatische Ether sind fast sämtlich nur unter ihrem Trivialnamen bekannt. | ||
| + | |||
| + | Beispiele: | ||
| + | * Die Verbindung H<sub>3</sub>C–O–CH<sub>3</sub> setzt sich zusammen aus einem H<sub>3</sub>C–O-Substituenten und dem Methyl-Rest (CH<sub>3</sub>) als Stamm, wobei hier allerdings beide Reste gleichwertig sind. Entsprechend heißt die Verbindung Methoxymethan oder Dimethylether: | ||
[[Datei:Dimethyl ether Structural Formulae.svg|zentriert|150px|Methoxymethan]] | [[Datei:Dimethyl ether Structural Formulae.svg|zentriert|150px|Methoxymethan]] | ||
| − | * H<sub>3</sub>C–O–CH(CH<sub>3</sub>)<sub>2</sub> heißt | + | * H<sub>3</sub>C–O–CH(CH<sub>3</sub>)<sub>2</sub> heißt 2-Methoxypropan oder Isopropylmethylether. Die höherrangige Propan-Kette bildet den Stammnamen, an die ein Methoxy-Substituent an 2- (bzw. ''iso''-) Position des Propylrestes gebunden ist: |
[[Datei:Methylisopropyl ether Structural Formulae.svg|zentriert|170px|2-Methoxypropan]] | [[Datei:Methylisopropyl ether Structural Formulae.svg|zentriert|170px|2-Methoxypropan]] | ||
| − | |||
| − | |||
| − | |||
Version vom 1. März 2017, 19:08 Uhr
Inhaltsverzeichnis |
Power to Gas
Alkohole
Definition: ...
Benennung der Alkohole
Eigenschaften der Alkohole
Methanol der Supertreibstoff
Datei:Fuel cell NASA p48600ac.jpg
Kleine Brennstoffzelle zur Gewinnung von Strom aus Methanol ohne Verbrennung
- Oktanzahl: 160
- Dichte Methanol: 0,79 kg/l
Fragen:
- Wieviel CO2 entsteht aus einem Liter Methanol
- 1 l Methanol bringt wieviel Energie?
Ether
Datei:Ether.png
Struktur und Bindungsverhältnisse der Ether
Allgemein kann ein Ether als
dargestellt werden. R1 und R2 sind hier Alkyl-Reste. Die Bindungsverhältnisse in Ethern ähneln denen in Alkoholen und im Wasser, das als Grundkörper dieser beiden Verbindungsklassen aufgefasst werden kann. Mit den zwei freien Elektronenpaaren am Sauerstoff führt es zu einer tetraedrischen Anordnung der vier Elektronenwolken bzw. zu einem Winkel am Sauerstoff. Der Bindungswinkel des Sauerstoffs ist aufgrund der gegenüber Wasserstoff (104,5° im H2O) voluminöseren Alkylsubstituenten mit 112° erweitert.
Benennung Ether
Gemäß der IUPAC-Nomenklatur werden aliphatische Ether als Alkoxy-Alkane bezeichnet: R1–O–R2
- Die die Gruppe O–R2 ist ein Alkoxy-Substituent einer Alkan-Kette R1 behandelt wird.
- Der niederrangigere Substituent der Kette ist hierbei der Alkoxy-Rest (–O–R2), der höherrangigere bildet den Stamm des Stoffnamens.
- Ebenfalls von der IUPAC zugelassene Namen werden durch Nennung der beiden Alkylreste und der Endung ether gebildet und sind besonders für kleine, aliphatische Ether gebräuchlich.
- Bei symmetrischen Ethern ist dann die Bezeichnung sehr einfach durch Vorstellen eines Di möglich [z. B.: Diethylether (Ethoxyethan) oder Dimethylether (Methoxymethan)]. Cyclische und aromatische Ether sind fast sämtlich nur unter ihrem Trivialnamen bekannt.
Beispiele:
- Die Verbindung H3C–O–CH3 setzt sich zusammen aus einem H3C–O-Substituenten und dem Methyl-Rest (CH3) als Stamm, wobei hier allerdings beide Reste gleichwertig sind. Entsprechend heißt die Verbindung Methoxymethan oder Dimethylether:
- H3C–O–CH(CH3)2 heißt 2-Methoxypropan oder Isopropylmethylether. Die höherrangige Propan-Kette bildet den Stammnamen, an die ein Methoxy-Substituent an 2- (bzw. iso-) Position des Propylrestes gebunden ist: