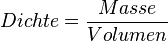Sauber und schön: Unterschied zwischen den Versionen
(→Löslich oder nicht löslich?) |
(→Löslich oder nicht löslich?) |
||
| Zeile 30: | Zeile 30: | ||
* <u>Milch</u> | * <u>Milch</u> | ||
| − | <center><gallery> | + | <center><gallery heights=250 widths=250> |
Datei:Milk glass.jpg|Von außen sieht man keine zwei Bestandteile | Datei:Milk glass.jpg|Von außen sieht man keine zwei Bestandteile | ||
Datei:Milkccar.jpg|... genauer betrachtet sieht man die Fetttröpfchen | Datei:Milkccar.jpg|... genauer betrachtet sieht man die Fetttröpfchen | ||
| Zeile 39: | Zeile 39: | ||
* <u>Lösungen von Salz oder Kohlendioxid in Wasser</u> | * <u>Lösungen von Salz oder Kohlendioxid in Wasser</u> | ||
<center> | <center> | ||
| − | <gallery> | + | <gallery heights=250 widths=250> |
File:90, Israel - panoramio.jpg|Nur am Rand sieht man, dass im Wasser des toten Meeres viel Salz gelöst ist. | File:90, Israel - panoramio.jpg|Nur am Rand sieht man, dass im Wasser des toten Meeres viel Salz gelöst ist. | ||
Teilchenmodell Lösung Salz.png|Die Ionen des Salzes sind im Wasser verteilt. | Teilchenmodell Lösung Salz.png|Die Ionen des Salzes sind im Wasser verteilt. | ||
| Zeile 52: | Zeile 52: | ||
* <u>Wasser und Öl</u> | * <u>Wasser und Öl</u> | ||
<center> | <center> | ||
| − | <gallery> | + | <gallery heights=250 widths=250> |
Datei:Öl-Wasser-Gemisch.jpg|Das Öl hebt sich deutlich vom Wasser ab. | Datei:Öl-Wasser-Gemisch.jpg|Das Öl hebt sich deutlich vom Wasser ab. | ||
Datei:Teilchenmodell Emulsion.png|Auf Teilcheneben ist es wie bei Milch, nur sind die Öl-Tropfen größer. | Datei:Teilchenmodell Emulsion.png|Auf Teilcheneben ist es wie bei Milch, nur sind die Öl-Tropfen größer. | ||
Version vom 23. September 2018, 20:18 Uhr
- Waschmaschine Historisch.jpg
Alte Waschmachine, die nach dem gleichen Prinzip funktioniert wie heute
- Bundesarchiv Bild 102-09247, Berlinerin im Schaumbad.jpg
Welche Bedeutung das Reinigungsmittel, wie Seife?
- Gewerbewaschmaschine.jpg
Chemische Reinigung?
- Rednails.jpg
Sauber oder nicht? Schön ... ?
- Жидкость для снятия лака.JPG
Manchmal muss auch der Nagellack weg!
|
Eine Reinigung geschieht dadurch das
|
Tipps für die richtige Reinigung: Cleanipedia mit Reinigungstipps passend zu jedem Fleck!
Inhaltsverzeichnis |
Löslich oder nicht löslich?
Zwei Stoffe sind ineinander löslich, wenn beim Vermischen ein homogenes Gemisch entsteht.
|
Beispiele:
- Milch
- Milk glass.jpg
Von außen sieht man keine zwei Bestandteile
- Milkccar.jpg
... genauer betrachtet sieht man die Fetttröpfchen
- Lösungen von Salz oder Kohlendioxid in Wasser
- 90, Israel - panoramio.jpg
Nur am Rand sieht man, dass im Wasser des toten Meeres viel Salz gelöst ist.
- Drinking glass 00118.gif
Die Kohlensäurebläschen verlassen aus der Lösung heraus!
- Wasser und Öl
| Ein Stoff ist in einem Lösungsmittel löslich, wenn die Teilchen des Stoffes einzeln im Lösungsmittel verteilt ist, denn einzelne Teilchen kann man nicht sehen. |
Damit sich die Teilchen des Stoffes im Lösungsmittel verteilen ...
muss die Anziehung der Teilchen des Stoffes überwunden werden. die Teilchen des Lösungsmittel müssen die Stoff-Teilchen umgeben und dadurch von den anderen trennen. Von Salz wissen wir, dass sich die Ionen, aufgrund der verschiedenen Ladungen sehr stark anziehen. Das Wassermoleküle haben allerdings hat den Vorteil, dass sie sich zu den Ionen hingezogen fühlen und dadurch sich eine stabile Schicht an Wasserteilchen rund um die Ionen bilden, die die Anziehung der Ionen untereinander aufhebt.
Daraus ergibt sich nun die Frage, warum Wasser das macht? Und warum lösen sich solche Stoffe wie Öl nicht in Wasser. Das können wir mit unserem bisherigen Wissen noch nicht erklären. Und darum soll es in diesem Themenabschnitt "Sauber und Schön" auch gehen.
Zum Abschluss der Wiederholung sollst du nun noch einmal die Begriffe zu den Gemisch-Typen üben und anwenden.
30px Aufgabe 1a
Übe den Begriff und homogen und das Gegenteil heterogen, indem du in einem Quiz jeweils bei einem Teilchenmodellbild entscheidest, ob man zwei Phasen erkennen kann oder nicht. |
30px Aufgabe 1b
Zur Wiederholung der Gemisch-Arten sortiere die Begriffe, die Aggregatzustände der Gemischbestandteile, das Teilchenmodell-Bild und ein Beispiel mit Beispiel-Bild. Halte dann die Informationen in einer Tabelle fest (senkrecht/waagrecht die Aggregatzustände), wobei du in jedem Feld ein Beispiel für ein homogenes und ein Beispiel für ein heterogenes Gemisch notieren sollst. |
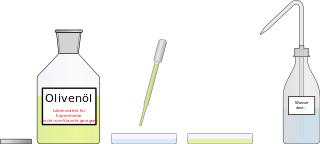
Experimente zum Mischen von Öl und Wasser
Hinweis: Öl ist eine recht zähflüssige Flüssigkeit, was die Nutzung mit einigen Geräten recht unpraktisch macht. Daher wird bei einigen Experimenten das Öl durch etwas ersetzt, was sich wie Öl verhält, aber dünnflüssiger ist.
30px Aufgabe 2
Macht euch Notizen zu den Experimenten entsprechend der Anweisungen, die jeweils bei den einzelnen Experimenten zu finden sind. Es ist Hausaufgabe, dies ordentlich ins Heft zu notieren. Die Nummern der Experimente sind egal, wichtiger ist die Überschrift! |
VERSUCH: 2. Ablenkung durch den Luftballon?
Materialien: Das Experiment ist schon vorbereitet. Falls die Gruppe vor euch vergessen hat, die Flüssigkeiten zurück in die Büretten zu gießen, dann macht dies und nutzt die kleinen Trichter dazu, die auf den Bürtten bleiben sollen. Natürlich sollte der Hahn unten geschlossen sein (steht quer). Außerdem ein aufgeblasener Lauftballon. Aufbau/Durchführung: Der Luftballon dient hier dazu, eine Ladung durch Reiben an einem Pulli/T-Shirt zu erzeugen. Das funktioniert am besten an Kunstfasern, geht aber auch mit Baumwoll-T-Shirts. Ob ihr eine Ladung habt, könnt ihr an frisch gewaschenen, nicht zu kurzen Haaren ausprobieren. Nachdem der Ballon aufgeladen wurde öffnet ihr bei einer der Büretten unten den Hahn und lasst einen feinen Flüssigkeitesstrahl heraus. Dieser sollte zunächst in das jeweilige Becherglas gelangen! Lasst euch nicht zu viel Zeit, damit nicht die ganze Flüssigkeit herausgelaufen ist! Haltet dann den gerade erst aufgeladenen Ballon neben den Flüssigkeitsstrahl ohne ihn zu berühren.
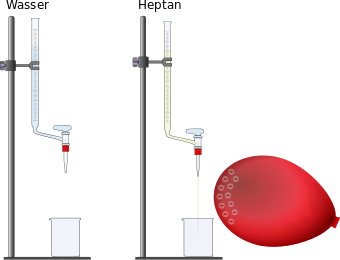 Aufgabe: Haltet in einer kurzen Skizze mit einer Beschreibung das Ergebnis des Experimentes unter der Überschrift "Ablenkung eines Wasserstrahls" im Heft fest. Entsorgung: Die herausgelaufenen Flüssigkeiten werden wieder in die jeweiligen Büretten eingefüllt. Dazu könnt ihr die Büretten auf den Boden stellen, damit man leichter an die Öffnung kommt. Die Bechergläser müssen nicht gereinigt werden. Falls in der Bürette mit dem Wasser zu wenig Wasser enthalten ist, einfach mit Wasser aus dem Wasserhahn nachfüllen, indem ihr euch mit dem Becherglas etwas holt. Nutzt die Trichter, damit nichts daneben geht! |
VERSUCH: 3. Was ist in was löslich?
Materialien: Reagenzglasständer mit 6 Reagenzgläser, 6 Gummistopfen, wasserlöslicher Folienstift, Spritzflasche mit destlilliertem Wasser, 1-Pentanol, Heptan, Ethanol, Papier zum Reinigen der Stopfen Aufbau/Durchführung: Ihr sollt untersuchen, wie gut sich die vier vorhandenen Chemikalien miteinander mischen. Diese 6 Mischversuche führt ihr in jeweils einem Reagenzglas durch. Beschriftet dazu die Reagenzgläser und haltet die verschiedenen Gemische darauf fest, damit ihr nicht den Überblick verliert. Gebt jeweils 1-2 cm der zwei Flüssigkeiten zusammen in das Reagenzglas, verschließt mit einem Stopfen und schüttelt ein wenig, um besser zu mischen. Lasst den Stopfen dann auf dem Reagenzglas und bereitet die nächste Mischung vor. 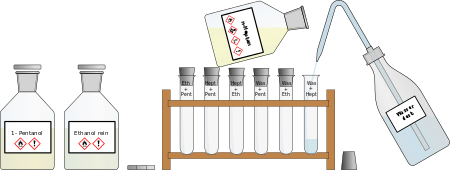 Aufgabe: Nachdem ihr alle Gemische hergestellt habt, haltet das Ergebnis unter der Überschrift "Mischversuche von Wasser mit verschiedenen Lösungsmitteln" fest, indem ihr eine Tabelle folgendermaßen anlegt. Notiert ein "+" , wenn die Stoffe sich miteinander so vermischen, dass man nur noch eine Phase sieht, notiert ein "-", wenn man sieht, dass sie sich nicht mischen lassen und sich zwei Phasen gebildet haben. 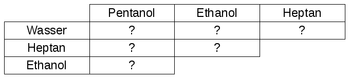 Entsorgung: Die Gemische werden in dem "Abfall-Becherglas" vorne am Lehrertisch gesammelt. Die Reagenzgläser werden nach dem Ausleeren in die Schüssel auf dem Lehrertisch eglegt, damit sie später gereinigt werden. Die Stopfen werden mit Papier abgewischt. |
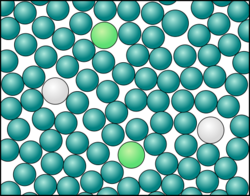
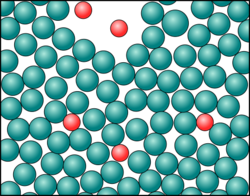
| VERSUCH: 4. Computer-Experiment: Simulation eines Wasser und Öl Gemisch
Aufbau/Durchführung: Öffne das Programm "SimChemistry" (siehe ....) und von dort aus die Datei "Wasser-Öl-Simulation", das im Verzeichnis "i" zu finden ist. Entsorgung: Schließt das Fenster mit der von euch verwendeten Simulation. Aufgabe: Die blauen Teilchen sind die Wasser-Moleküle, sie haben fest definierte Eigenschaften. Die gelben Teilchen stehen für Teilchen von Öl oder anderen Lösungsmittel. Bei diesen Teilchen kannst du zwei Einstellungen vornehmen.
Verändert die Einstellungen und wartet kurze Zeit, was sich verändert. Sucht verschiedene Einstellungen, bei denen sich die Teilchen mischen bzw. auftrennen. Skizziert dies im Heft und haltet dazu fest, welche Einstellungen vorliegen. |
30px Aufgabe 3
Informiere dich über die Schmelz- und Siedetemperaturen der beteiligen Stoffe an den Experimenten. Halte die Werte in einer Tabelle fest. Dies wird später gebraucht. Vielleicht fällt dir aber schon etwas auf!? |
Lösungsmittel unter der Lupe
Öle sind recht komplizierte Verbindungen und haben große Moleküle. Sie zu beachten und zu verstehen, warum Wasser und Öl so unterschiedlich sind, lenkt von dem eigentlichen Problem ab. Wir beachten daher eine Gruppe von Verbindungen, die sich gut mit Öl vermischen und daher ähnliche Eigenschaften haben. Im Gegensatz zum sind die Moleküle aber recht einfach aufgebaut.
Alkane - gesättigte Kohlenwasserstoff
| Kohlenwasserstoffe sind Verbindungen, deren Moleküle nur aus Kohlenstoff- und Wasserstoffatomen bestehen. Der einfachste Vertreter ist das Methan. |
Als Alkane bezeichnet man Kohlenwasserstoffe, bei denen sich die Atome immer nur jeweils ein Elektronenpaar teilen, dass sie zusammenhalten (Einfachbindung). Dagegen haben die Kohlenstoffatome bei Alkene auch mal vier gemeinsame Elektronen, sie haben Doppelbindungen.
|
30px Aufgabe 4
Informiere dich im Buch über die Alkane. Halte unter der Überschrift "Alkane" im Heft wichtige Informationen fest. Beachte dabei die Aufgabe 4, damit du weißt, was du da machen musst.
|
30px Aufgabe 5
Halte im Heft unter der Überschrift Homologe Reihe Alkane, die ersten 10 Alkane tabellarisch fest. Suche auch nach ihren Siedetemperaturen und halte sie in der letzten Spalte fest Lerne die Namen und die Formeln auswendig.
|
| Namen | Summenformeln | Lewissschreibweise | Siedetemperatur |
|---|---|---|---|
| Methan | 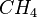 |
80px | -161°C |
| Ethan | ... | ... | ... |
| ... | ... | ... | ... |
}}</center>
30px Aufgabe 6
Übe die Namen und Formeln der ersten Alkane mit Hilfe der zwei Quizze: |
Verzweigt und verzwickt?
Die Struktur (also wie die Atome aneinander hängen) bei den Alkanen scheint verhältnismäßig einfach und klar, aber ab 4 Kohlenstoffatomen taucht ein kleines Problem auf. Das sollst du mit Hilfe des Molekülbaukastens genauer erkunden.
| Ein Molekülbaukasten dient im Chemieunterricht zur Veranschaulichung von Molekülverbindungen. Die verschiedenen Atome werden dabei durch verschiedenfarbige Kunststoffkugeln dargestellt, die mit Hilfe von Verbindungsstücken zusammengestckt werden können. |
30px Aufgabe 7
Baue mit dem Molekülbaukasten die folgenden einfachen Moleküle nach:
|
30px Aufgabe 8a
Schauen dir die Kugeln der folgenden Elemente einmal genauer an:
|
30px Aufgabe 8b
In einer anderen Baukasten-Variante sind auch Schwefelatome enthalten. Vergleiche deine Ergebnisse aus Aufgabe 7a mit dem, was du beim Schwefelatom siehst. Wie ist das erklärbar? |
30px Aufgabe 9
Nimm dir die zweimal die Atome, die du zum Bauen von Butan brauchst (also 4xC und 10xH mit entsprechenden Bindungen).
|
Was macht den Unterschied zwischen einem Wasser und einem Methan-Molekül?
Wie wir schon bei den Siedetemperatur gesehen haben, hat Wasser im Vergleich zu Methan eine sehr viel höhere Temperatur, die sich nicht mit dem Gewicht erklären lässt. Die Experimente haben ja auch gezeigt, dass Wasser-Moleküle sich anziehen müssen. Ionen können allerdings nicht vorliegen, denn sonst wäre Wasser eher eine feste Verbindung. Woher die hohe Siedtemperatur kommt wollen wir nun erklären.
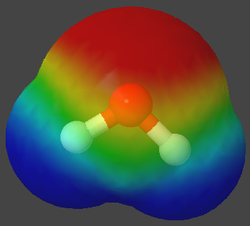
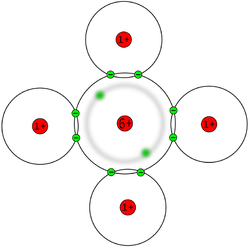
Die folgenden Bilder zeigt spezielle Ansichten von einem Wasser- und einen Methan-Molekül. Dabei wird die Verteilung der Elektronen in den Hüllen der Atome angezeigt. Wobei mit den Farben gezeigt wird, ob ein relativer Elektronenmangel oder -überschuss herrscht.
Um es noch mal zu betonen: hier hat keine echte Ionisierung stattgefunden! Durch eine ungleiche Verteilung der Elektronen
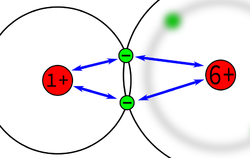
Um die Verteilung der Elektronen erklären zu können, wollen wir an einer Schalenmodelldarstellung vom Methan noch einmal erklären, wie die Atombindung zustande kommt.
Die Anziehung der Bindungselektronen ist bei den verschiedenen Atome unterschiedlich stark. Die Anziehung hängt ab von
|
Diese Anziehung kann man experimentell bestimmen und dass hat zu eine Liste von Zahlen geführt, den sogenannten Elektronegativitäten.
Die Elektronegativität ist ein Maß für die Fähigkeit eines Atoms, die Bindungs-Elektronen an sich zu ziehen.
|
| IUPAC-Gruppe | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Periode | |||||||||||||||||||
| 1 | H 2,20 |
He | |||||||||||||||||
| 2 | Li 0,97 |
Be 1,47 |
B 2,01 |
C 2,50 |
N 3,07 |
O 3,50 |
F 4,17 |
Ne | |||||||||||
| 3 | Na 1,01 |
Mg 1,23 |
Al 1,47 |
Si 1,74 |
P 2,06 |
S 2,44 |
Cl 2,83 |
Ar | |||||||||||
| 4 | K 0,91 |
Ca 1,04 |
Sc 1,20 |
Ti 1,32 |
V 1,45 |
Cr 1,56 |
Mn 1,60 |
Fe 1,64 |
Co 1,70 |
Ni 1,75 |
Cu 1,75 |
Zn 1,66 |
Ga 1,82 |
Ge 2,02 |
As 2,20 |
Se 2,48 |
Br 2,74 |
Kr | |
| 5 | Rb 0,89 |
Sr 0,99 |
Y 1,11 |
Zr 1,22 |
Nb 1,23 |
Mo 1,30 |
Tc 1,36 |
Ru 1,42 |
Rh 1,45 |
Pd 1,30 |
Ag 1,42 |
Cd 1,46 |
In 1,49 |
Sn 1,72 |
Sb 1,82 |
Te 2,01 |
I 2,21 |
Xe | |
| 6 | Cs 0,86 |
Ba 0,97 |
La 1,10 |
Hf 1,23 |
Ta 1,33 |
W 1,40 |
Re 1,46 |
Os 1,52 |
Ir 1,55 |
Pt 1,44 |
Au 1,42 |
Hg 1,44 |
Tl 1,44 |
Pb 1,55 |
Bi 1,67 |
Po 1,76 |
At 1,96 |
Rn | |
| 7 | Fr 0,86 |
Ra 0,97 |
Ac |
Rf |
Db |
Sg |
Bh |
Hs |
Mt |
Ds |
Rg |
Cn |
Nh |
Fl |
Mc |
Lv |
Ts |
Og | |
30px Aufgabe 10
Suche für die Atome, die beim Wasser und beim Methan vorkommen, die Elektronegativitätswerte heraus und notiere sie dir so:
|
30px Aufgabe 10
Markiere hier bei dem Wasser- und bei dem Methanmolekül, zu welchen Kern die Bindungselektronen (also die Striche zwischen den Atomen) gezogen werden. Male dazu auf die Bindungsstriche Pfeile. |
| Ein Dipol ... |
Gleiches löst sich in Gleichem
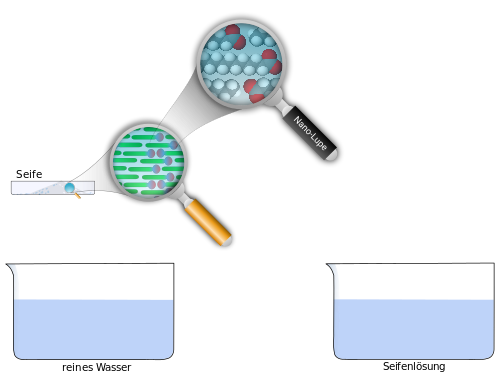
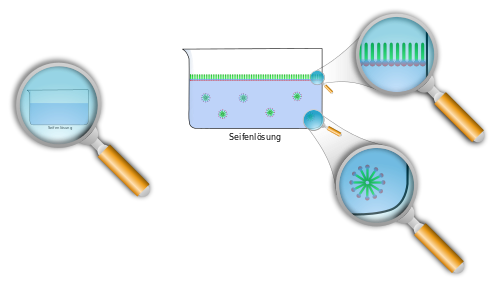
Wasser ist etwas Besonderes!
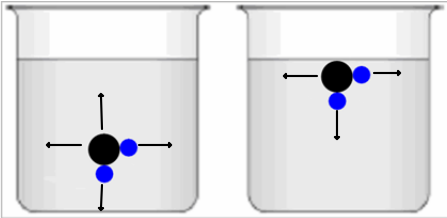
Oberflächenspannung
Betrachtet man die Siedetemperaturen von verschiedenen Wasserstoff-Verbindungen, so zeigt sich deutlich die Wirkung der Wasserstoffbrückenbindung und ihre Auswirkung auf die Werte.
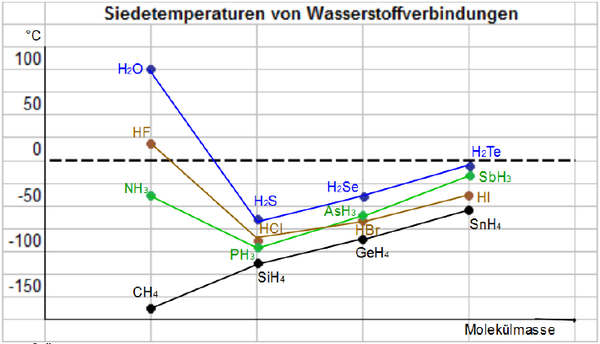
Eine kleine Amination, um die Wirkung der Wasserstoff-Brücken-Bindung zu zeigen:
 Datei:WassermoleküleInTröpfchen-2.svg
Datei:WassermoleküleInTröpfchen-2.svgWeitere Bilder zur Oberflächenspannung:
Übrigens gibt es noch einen Stoff, der eine höhere Oberflächenspannung hat als Wasser, nämlich Quecksilber. Man erkennt dies an den typischen runden Tröpfchen, die Quecksilber auch auf einem Untergrund ausbildet.
Dar Grund für die diese hohe Oberflächenspannung ist aber nicht eine Wasserstoffbrückenbindung. Vielmehr hat es damit zu tun, dass Quecksilber ein Metall ist. De Zusammenhalt der einzelnen Atome geschieht durch eine sogenannte Metallbindung, bei der sich quasi eine Kugelwolke um alle Atomkerne bildet.
Die Flash-Lerngeschichte 15px Die Oberflächenspannung des Wassers erläutert die Ursache der Oberflächen-Spannung noch einmal ausführlich.
Dichteanomalie des Wassers
Das Eis, also gefrorenes Wasser, auf flüssigem Wasser schwimmt, erscheint und normal. Tatsächlich ist Wasser da eine Ausnahme. Dazu ein Film:
Man vergleicht im Film das Verhalten von Wasser, mit Wachs und Eisessig (99%iger Essig). Weil die Dichte von Eis geringer ist als die Dichte des umgebenden Wassers, kann es im Wasser schwimmen. Beim Wachs und beim Eisessig ist es anders. Die Dichte der beiden Feststoffe ist größer als die der entsprechenden Flüsigkeiten und deshalb gehen sie unter.
Wasser zeigt damit eine Besonderheit, wenn man die Dichte bei verschiedenen Temperaturen betrachtet. Eine Besonderheit, die es bei keinem anderen Stoff in der Art gibt. Üblicherweise ist es so, dass sich die Dichte eines Stoffes bei sinkender Temperatur erhöht. Grund dafür ist, dass die Teilchen bei sinkenden Temperaturen immer langsamer werden und dadurch näher zusammenrücken können. Da sich dabei das Volumen verringert, wird die Dichte größer, denn die Dichte wird ja berechnet durch
Bei Wasser ist das nicht so. Es hat seine höchste Dichte bei 4°C. Dagegen ist die Dichte bei festem Wasser, also Eis, sehr viel geringer. Hexan zum Beispiel verhält sich "normal". Man erkennt, dass die Dichte sich mit der Temperatur kontinuierlich verändert: Je wärmer, desto kleiner wird die Dichte, denn bei einer schnelleren Bewegung brauchen die Teilchen mehr Platz, das Volumen vergrößert sich und so wird der Bruch kleiner.
| Die Tatsache, dass gefrorenes Wasser, also Eis, nicht absinkt ist von wesentlicher Bedeutung für das Überleben auf der Erde. Denn nur so können im Winter die Wasserbewohner überleben. Denn ist das Wasser tief genug, so friert ein Gewässer nicht durch und unten bildet sich eine 4°C kalte Schicht, in der die Wasserbewohner überleben können. | Datei:Anomalous expansion of water Summer Winter.svg |
Auch dieses Wasserphänomen lässt sich mit Hilfe der Wasserstoffbrücken erklären. Dazu der folgende Film, der den Übergang zwischen Wasser zu Eis dynamisch in Bewegung zeigt.
Erklärung: Beim Abkühlen bewegen sich die Wassermoleküle immer langsamer. Die relativ starke Wasserstoffbrücken-Bindung bewirkt die Anordnung der Moleküle in dem sechseckigen Wabengitter. Wird dagegen wieder erhitzt, so wird die Bewegung der Teilchen zu schnell, das Gitter zerfällt und die Wassermoleküle haben keinen festen Platz mehr. Sie sind enger beieinander und so hat das Wasser bei einer Temperatur knapp über dem Gefrierpunkt ein höhere Dichte (also kleineres Volumen). Beim Abkühlen nehmen die Wassermoleküle wieder von alleine die Position im Wabengitter ein.
Die zwei folgenden drehbaren Zeichnungen zeigen einmal Eis und zum anderen Wasser-Moleküle, die in Bewegung sind.
|
Ein bewegliches Bild bekommst du auf der Unterseite (denn leider kann die Extension zur Darstellung von 3D-Molekülen im Moment nur ein Bild pro Seite darstellen). Erklärungen: Man sieht eine recht große Anzahl an Wassermolekülen. Sie sind regelmäßig angeordnet, was sich daraus ergibt, dass je ein Wasserstoff-Atom mit einem der freien Elektronenpaare des Sauerstoff eines anderen Wassermoleküls über eine Wasserstoffbrücke miteinander "verbunden" sind. Diese starre Anordnung würde es aber in Realität nicht geben, da die Teilchen auch im gefrorenen Zustand immer ein wenig in Bewegung sind und auf der Stelle schwingen. Die Wasserstoffbrücken halten die Wassermoleküle aber trotzdem an der Stelle und bewirken die regelmäßige Anordnung. Die Wasserstoffbrücken sind hier noch nicht zu sehen, so können aber sichtbar gemacht werden.
Man hat eine Struktur, die von einigen Seiten sechseckige Löcher zeigt. Man also große Lücken, wodurch das Volumen größer und die Dichte geringer ist, als wenn die Moleküle beim flüssigen Wasser quasi lückenlos aneinander liegen. WICHTIG: Die hier zu sehende Darstellung, dass die Moleküle einen großen Abstand voneinander haben, ist natürlich alles andere als realistisch. Die hier zu sehende sogenannte Kugel-Stab-Darstellung kann man so verstehen, dass die Kugeln für die Atomkerne stehen, die Stäbe für die Bindungen. Tatsächlich haben wir ja bei den Atombindungen eine Überlagerung der Atomhüllen. Dies wird besser in einer anderen Darstellung, dem sogenannten Kalottenmodell verdeutlicht. Ein einzelnes Wassermolekül sieht dann so aus, wie im Bild rechts. Die Wassermoleküle hier kann man auch alle im Kalottenmodell anzeigen lassen.
Nun sieht man, dass sich die Moleküle tatsächlich alle berühren. Man kann kaum zwischen der Bindung zwischen den Atomen und den Wasserstoffbrückenbindungen unterscheiden. Trotzdem sind immer noch Lücken vorhanden! Download der CML-Datei, um sie im Programm Avogadro genauer anschauen zu können. | ||
| Hier ist auch wieder eine gewisse Anzahl an Wassermoleküle zu sehen und wie sie angeordnet wären, wenn das Wasser im flüssigen Zustand wäre. Es empfiehlt sich gleich, ins Kalottenmodell umzuschalten, damit man eine realistische Vorstellung hat.
Auch hier berühren sich die Moleküle und sieht man auch Lücken zwischen den einzelnen Molekülen, aber die Anordnung ist nicht regelmäßig und man kann nicht durchsehen. Die Dichte ist in diesem Zustand höher als beim Eis, da weniger Lücken vorhanden sind. Die gleiche Zeichnung, bei der die Moleküle in Bewegung sind, ist hier zu sehen. |
Eine weitere Darstellung für den Übergang zwischen Wasser und Eis wird auf dieser Seite gezeigt.
| 50px | Im Buch zu lesen: Zum Thema Wasserstoffbrückenbindung und Dichteanomalie findest du in unserem Buch Informationen auf den Seiten 221 und 222. |