Einstieg in die Chemie: Unterschied zwischen den Versionen
(→Aggregatzustände im Teilchenmodell) |
(→Aggregatzustände im Teilchenmodell) |
||
| Zeile 569: | Zeile 569: | ||
::''In einem Video wird der Lösungsvorgang simuliert.'' | ::''In einem Video wird der Lösungsvorgang simuliert.'' | ||
| + | == Stoffe verändern sich - chemische Reaktionen == | ||
| + | |||
| + | Wir haben die Eigenschaften von Stoffen untersucht und diese Stoffeigenschaften genutzt, um sie zu unterscheiden. | ||
| + | |||
| + | Es kann aber vorkommen, dass ein Stoff sich verändert, das er neue Eigenschaften bekommt. Das kann langsam gehen oder schnell: | ||
| + | * Eisen rostet mit der Zeit, es ist eine sehr langsame Veränderung, die unspektakulär ist. | ||
| + | * Magnesium verbrennt, wenn man es anzündet mit heller Flamme. Es bleibt ein weißes Pulver zurück. | ||
| + | |||
| + | {{AufgabeNr|16|Überlege, warum wir davon ausgehen können, dass hier jeweils neue Stoffe entstanden sind.}} | ||
| + | |||
| + | {{Kurzregel|Eine '''chemische Reaktion''' ist ein Vorgang bei dem '''Ausgangsstoffe''' verschwinden und neue Stoffe erscheinen. Dies kann man anhand der Eigenschaften erkennen.} } | ||
| + | |||
| + | <gallery widths="400" heights="300" style="text-align:center" caption="Magnesium vor und nach der Verbrennung"> | ||
| + | File:Magnesium-products.jpg|Magnesium ist ein helles, silberglänzendes Metall. | ||
| + | File:Magnesium ribbon burning.jpg|Wenn man es anzündet, brennt es mit sehr heller Flamme. Es steigt weißer Rauch auf was aber nur das verbrannte Magnesium ist, dass zurückbleibt, wenn die Flamme ausgegangen ist. | ||
| + | Datei:Magnesium_oxide.jpg|Weißer Rückstand der Magnesiumverbrennung. | ||
| + | </gallery> | ||
| + | |||
| + | {{Kurzregel|'''Chemische Reaktionen''' sind meist mit einem Umsatz an Energie verbunden. Es wird Energie frei oder man muss Energie hinzufügen.}} | ||
| + | |||
| + | |||
| + | {{Kurzregel|<u>Zusammenfassung:</u> ''Eine chemische Reaktion ist ein Vorgang bei dem es zu einem Umsatz von Stoffen und Energie kommt.''}} | ||
| + | |||
| + | <u>Dies soll noch einmal erklärt werden:</u> | ||
| + | |||
| + | * '''Stoffumsatz:''' In diesem Fall bedeutet das, das die Ausgangsstoffe scheinbar verschwinden und dann stattdessen der neue Stoff vorhanden ist. Die Ausgangsstoffe werden also bei der chemischen Reaktion verbraucht. | ||
| + | * '''Energieumsatz:''' Dies kann unterschiedlich sein. Im Beispiel von bei der Verbrennung Magnesium heißt es, dass die Reaktion unter Energieabgabe stattfindet, auch wenn man am Anfang erhitzen muss, bis die Reaktion startet. Bei anderen Reaktionen muss man dauerhaft erhitzen, damit die Reaktion stattfindet. Beim Rosten von Eisen ist es eine sehr langsame Reaktion bei der auch Energie frei wird. Da die Reaktion aber langsam ist, merkt man keine Erwärmung. | ||
| + | |||
| + | {{AufgabeNr|17|Fallen dir aus dem Alltag und im Haushalt chemische Reaktionen ein. Überlege jeweils und halte fest: | ||
| + | * Welches sind die Ausgangsstoffe und was die Endstoffe? Welche Eigenschaften haben sich geändert? | ||
| + | * Musste der Ausgangsstoff/die Ausgangsstoffe die ganze Zeit erwärmt werden oder wird Energie (Wärme, Licht) frei? | ||
| + | }} | ||
| + | |||
| + | === Was müsste bei einer chemischen Reaktion im Teilchenmodell passieren. | ||
| + | |||
| + | <center><iframe width="1280" height="720" src="https://www.youtube.com/embed/h4wu3s5y7Dw?rel=0&showinfo=0" frameborder="0" allowfullscreen></iframe></center> | ||
| + | |||
| + | {{AufgabeNr|18| | ||
| + | }} | ||
<!-- Unsichtbar :-) --> | <!-- Unsichtbar :-) --> | ||
[[Kategorie:Rheinland-Pfalz]] | [[Kategorie:Rheinland-Pfalz]] | ||
Version vom 12. Januar 2016, 16:44 Uhr
Was ist eigentlich Chemie?
| 350px | Wenn du überlegst, was du dir unter einem Chemiker so vorstellst, wirst du vielleicht bei einem solchen Bild, wie das links, sofort zustimmen ... das sieht nach einem Chemiker aus, oder? |
Die Frage, was Chemie eigentlich genau ist, wirkt im ersten Moment ganz einfach. Ein Chemiker oder ein Chemielehrer sollte sie doch ohne weiteres beantworten können! Aber leider ist die Antwort auf diese Frage alles andere als klar. Und trotzdem versuchen wir, ein wenig Licht in das Dunkel zu bringen. Ein berühmter Chemiker soll einmal folgendes gesagt haben:
|
“Chemie
19px Linus Pauling , Nobelpreis für Chemie 1954 |
Die Wissenschaft Chemie beschäftigt sich also ganz grundlegend mit all den Dingen, die uns umgeben. Woraus bestehen diese Dinge? Welche Eigenschaften haben sie - und warum? Wie kann ich Stoffe ineinander umwandeln, also zum Beispiel aus Sand Glas erzeugen?
Was machen Chemiker?
Chemie spielt in vielen Bereichen des Alltags eine herausragende Rolle:
| Chemiker können gezielt neue Stoffe "erfinden". |
- In der Materialwissenschaft werden z.B. Kunststoffe mit bestimmten benötigten Eigenschaften hergestellt. Wegen drohender Erdölknappheit, muss man sich überlegen, wie man Kunststoffe aus Naturstoffen herstellen kann. Auch die Entsorgung und das Recycling sind dabei wichtig.
| |
|
|
| Das sogenannte 19px Aerogel ist besonders leicht aber trotzdem stabil. Ein 2,5 kg schwerer Ziegel wird hier von einem 2 g schweren Stück Aerogel getragen. | Thermoplastische Polyurethane sind neue, gut federnde und gut wieder verwertbare Materialien für die Sohlen von Sportschuhe. | 19px Graphen ist ein "neuer" Wunderstoff, von dem man sich viel verspricht. Nur eine Lage von Kohlenstoff-Atomen sind besonders gut leitfähig. An Anwendungen forscht man noch. |
| Chemiker forschen an den Batterien von morgen. |
- Ein wichtiger Punkt im Alltag ist die Energie. Energie muss gespeichert werden, die mit Hilfe von Sonne und Wind produziert wird. Das kann in Form von energiereichen Stoffen geschehen, wenn etwa aus Wasser das brennbare Gas Wasserstoff produziert wird. Oder in Form von Batterien, bei denen es zum Beispiel für Elektroautos darum geht, dass die Akkus lange halten und schnell geladen werden können.
| |
|
|
|
| Der durch Solar- oder Windenergie produzierte Wasserstoff kann zwar direkt als Brennstoff verwendet werden, ... | aber als Methan-Gas lässt er sich besser transportieren. | Oder man produziert die Flüssigkeit Methanol, die sich wie Benzin tanken lässt. | 19px Redox-Flow-Batterie sind relativ neu. Man lädt sie nicht auf, sondern tauscht den Elektrolyten aus, um wieder Energie zu haben. |
| Chemiker analysieren die Umwelt auf Gifte oder die Reinheit wichtiger Stoffe. |
- Die Analyse der Umwelt ist wichtig, denn die Chemiker kennen Methoden um Gifte und die Zusammensetzung von Stoffen bestimmen zu können. Dies spielt bei der Kontrolle von Lebensmitteln (auch Wasser) und etwa Arzneimittel eine große Rolle.
| |
|
|
| Einfache Handversuche kann man verwenden, um schnell das Vorhandensein von Stoffen nachzuweisen. | Diese einfache Chromatographie, kann man auch zu Hause durchführen. | In größeren Laboren verwendet man allerdings eher Geräte, wie diese Gaschromatographen. |
30px Aufgabe 1
Lies im Schulbuch die Seite 13 und beantworte schriftlich im Heft die Aufgaben 1-3. Überschrift bitte darüber schreiben!! |
Laborgeräte
Damit du Experimentieranleitungen nutzen kannst, musst du die Namen der Geräte kennen, die dort genannt werden. Du musst die Namen der Geräte auswendig lernen und auch aufgrund des verwendeten Material verstehen, für was man ein Gerät verwenden kann und für was nicht.
Die Namen der Geräte
30px Aufgabe 2
Nutze im Buch die Seite 7, um das Arbeitsblatt (Anschauen oder Herunterladen) so weit wie möglich auszufüllen. Die restlichen Namen werden im Unterricht geklärt. |
Eine ausführliche Liste liefert der Wikipedia-Artikel 19px Laborgerät .
30px Aufgabe 3
Kennst du die Namen der Laborgeräte? Übe sie hier beim Zuordnungsquiz. |
Das Material der Laborgeräte
Die meisten Laborgeräte bestehen aus den folgenden Materialien:
- 19px Holz - 19px Eisen - 19px Glas - 19px Plastik ... leider sind die Wikipedia-Artikel recht kompliziert zu lesen!
- أنابيب اختبار.jpg
Reagenzgläser im Reagenzglasständer
- Messkolben.jpg
Messkolben
- Propipetta.jpg
ein Peleusball
- Pinzetten gr.jpg
Pinzetten
Dabei ist die Auswahl nicht willkürlich, denn man verwendet natürlich das Material für ein Gerät, dass am besten zu den Anforderungen passt. Oder man hat verschiedene Varianten aus verschiedenen Materialien: gerade Plastik wird gerne verwendet, wenn etwas nicht zu viel beansprucht wird, aber leicht und billig sein soll.
Welche Vor- und Nachteile diese Materialien genauer haben, sollst du in den folgenden Quizzen entdecken. Dabei kannst du überprüfen, ob du dich schon gut auskennst!
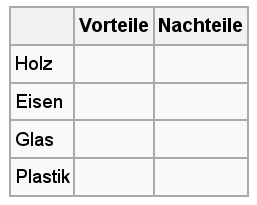
30px Aufgabe 4
Ordne die Vor- und Nachteile des jeweiligen Stoffe richtig zu und halte das richtige Ergebnis als Tabelle im Heft fest. |
Beweise dein Können und versuche die Millionen-Frage zu knacken! Hier geht es zum Quiz.
Chemie beschäftigt sich mit Stoffen. Was sind Stoffe aber genau?
| Das sind natürlich Stoffe in der Chemie | ... und was ist damit? |
| 300px | 360px |
Stoffe sind all die Materialien, aus denen unsere Welt zusammengesetzt ist. Wieviele Stoffe es genau gibt, kann man vermutlich nicht sagen, aber eine wichtige chemische Organisation gibt schon mal mindestens 30 Millionen als Anzahl an.
Bisher haben wir uns, bei der Betrachtung der Laborgeräte, mit vier Materialien beschäftigt. Nicht alle davon kann man aber als chemischen Stoff bezeichnen. Und zwar ist das Holz - ein natürliches Material - eben kein reiner Stoff sondern ein Gemisch, dass zum Beispiel auch Wasser enthält und das Lignin. Und je nachdem, welche Sorte Holz man hat, sind dessen Eigenschaften recht unterschiedlich. Das ist für Chemiker zu ungenau. Und das gilt für alle Naturstoffe, weswegen man diese meist in der Chemie nicht als Beispiele nimmt.
Nun aber mal wirklich genauer: was sind chemische Stoffe?
Stoffe im chemischen Sinne
Ein chemischer Stoff ist ein Material oder allgemein alles in den Naturwissenschaften, was man man beobachten und untersuchen kann und auch eine Masse besitzt. Raumbereiche, die keine Materie enthalten, bezeichnet man als Vakuum. Elektromagnetische Wellen, wie zum Beispiel Licht werden ebenfalls nicht zur Materie gezählt. Umgangssprachlich werden chemische Stoffe auch mit dem Wort Substanz bezeichnet, das im Sprachgebrauch der Chemie aber auf Stoffe in fester Form, sog. Feststoffe, beschränkt ist. Sonst hat man Flüssigkeiten oder Gase.
Stoffe in der Chemie werden grob unterschieden in Reinstoffe (Elemente oder Verbindungen) und Gemische. Es gibt weitere Unterteilungen, zu denen wir dann später noch kommen werden.
Wichtige Reinstoffe in der Chemie, die du schon kennen wirst, sind z. B. Wasser, Kochsalz (Natriumchlorid), Eisen, Alkohol (Ethanol)
Wichtige Stoffgemische sind zum Beispiel Luft, Salzsäure, Natronlauge (wie auf den Laugenbrezeln), Bronze, uvm.
Jede Stoffportion besitzt eine Masse, hat ein Volumen (also einen Platzbedarf) und besitzt eine innere Energie bzw. Wärmeenergie. Die Form eines Körpers kann auch bei gleichem Stoff (Material) unterschiedlich sein (z. B. Eisendraht, -pulver, -blech, -kugeln, -wolle).
Merke dir folgendes:
|
30px Aufgabe 5
|
Stoffeigenschaften
Eine Stoffeigenschaft ist eine, für einen bestimmten Stoff, typische Eigenschaft. Sie kann mit den Sinnen wahrgenommen werden (z. B. der Geruch) oder nur mit Messgeräten erfassbar sein.
In der Chemie unterscheidet man Reinstoffe von Stoffgemischen, denn Reinstoffe haben immer die gleichen Eigenschaften, während bei Stoffgemischen die Eigenschaften von den Mischungsverhältnissen der Komponenten abhängen.
Wie du schon bei den Laborgeräten feststellen konntest, sind die Stoffeigenschaften wichtig für deren Anwendung. Wir werden aber bald noch eine wichtige Bedeutung kennenlernen.
30px Aufgabe 6
Sammelt in Gruppen - in die ihr im Unterricht eingeteilt werdet - gemeinsam Stoffeigenschaften. Öffnet dann bitte nur den einen Link, der zu eurer Gruppe gehört. WICHTIG: Löscht nicht die Einträge von anderen Schülern (höchstens Rechtschreibefehler korrigieren)! Wenn ihr einige zusammen habt, sortiert die Eigenschaften. |
| Eine Stoffeigenschaft ist eine für einen bestimmten Reinstoff typische Eigenschaft. Sie kann mit den Sinnen wahrgenommen werden oder nur mit Messgeräten erfassbar sein.
Eine Stoffeigenschaft hängt nicht ab ...
|
Wenn man die von euch genannten Eigenschaften etwas sortiert und fachlicher formuliert, dann haben wir das da bisher:
| Physikalische Stoffeigenschaften | Chemische Eigenschaften | Physiologische Eigenschaften |
|---|---|---|
|
Werte, welche durch Messung und Experimente bestimmt werden. |
Verhalten in chemischen Reaktionen. |
Wahrnehmungen oder Auswirkungen auf die Umgebung |
|
|
|
30px Aufgabe 7
|
Probiere es aus!? Verstehst du schon die Begriffe und die gefährlichen Eigenschaften dieser Stoffe? Probiere es im Zuordnungs-Quiz aus!
Nutzung der Stoffeigenschaften zur identifizierung eines unbekannte Stoffes
Vergleich mit 5 weißen, pulverförmigen Feststoffen
Gegeben ist ein unbekannter weißer Feststoff, der pulverförmig ist. Es kommen fünf verschiedene Stoffe in Frage, die wir kennen. Das sind:
- Vitamin C
- Natron
- Backpulver
- Zucker
- Salz
30px Aufgabe 8
Überlege dir Eigenschaften, mit denen du diese Stoffe unterscheiden könntest. Finde also jeweils typische Eigenschaften. |
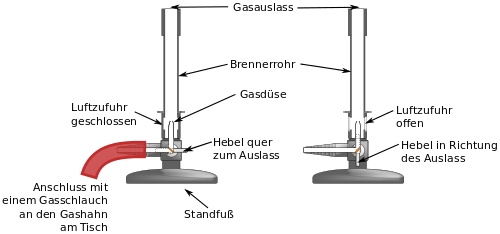
Kennenlernen des Bunsenbrenners
30px Aufgabe 9
Beschrifte das ausgeteilte Arbeitsblatt, um die Bestandteile des Bunsenbrenners kennenzulernen. Nutze dazu das Buch auf Seite 18 - V1. |
Die verschiedenen Brenner-Arten auch von innen:
 |
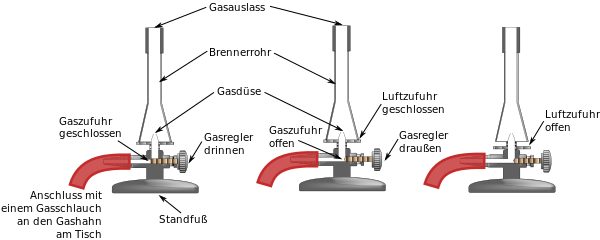
|
| |
|
30px Aufgabe 10
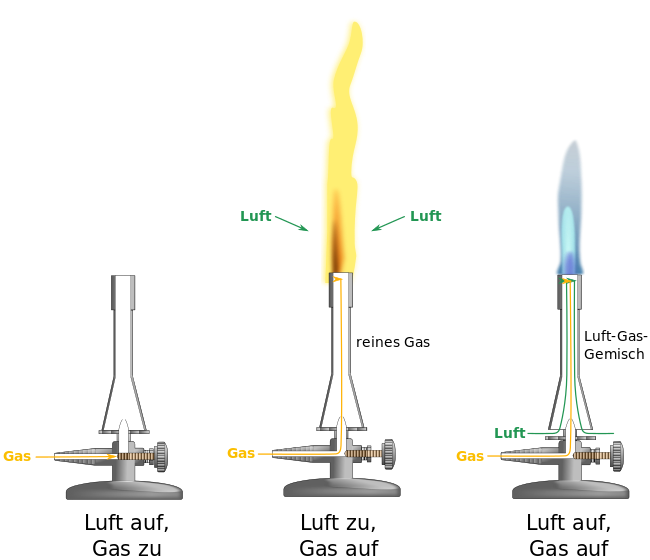
Zünde entsprechend der Anleitungen auf dem Arbeitsblatt und dem Buch (S. 18 - V 1) den Bunsenbrenner an. Jeder sollte das mindestens zweimal gemacht haben. |
30px Aufgabe 11
Untersuche die Flamme mit und ohne Luftzufuhr: Halte das Magnesiastäbchen in die verschiedenen Flammen. |
Warum dieser Unterschied mit und ohne Luft?
Experimente zur Untersuchung des (noch) unbekannten, weißen Feststoffes
| Sicherheitsinformationen für Experimente | ||
|---|---|---|
|
An Materialien wird benötigt:
- x saubere Reagenzgläser
- 1 schmutziges Reagenzglas
- Reagenzglasständer, Reagenzglashalter
- Gummistopfen, Spatel
Die folgenden Experimente sollen durchgeführt werden. Zu jedem Experiment gibt es auf einer Unterseite vertiefende Informationen
| VERSUCH: 1. Verhalten beim Erhitzen
Durchführung: Holt euch ein gebrauchtes Reagenzglas vom Lehrertisch. Gebt mit einem Spatel nicht mehr als 1 cm eures Stoffes in das gebrauchte Reagenzglas und erhitzt es über dem Bunsenbrenner. Achtet auf die besprochenenen Sicherheitsmaßnahmen. Erhitzt wie auch beim Wasser erst vorsichtig und wenn nichts passiert stärker. Allerdings muss das Reagenzglas nicht geschmolzen werden, um sagen zu können, dass der Stoff sich beim Erhitzen nicht verändert. Entsorgung: Versucht nach dem Abkühlen den Inhalt auszuschütten. Wenn das geht und Reste im Reagenzglas übrig bleiben, bitte gut mit Wasser und einer Bürste ausspülen. Kann der Inhalt nicht entfernt werden, bitte das Reagenzglas vorzeigen, damit ich entscheiden kann, ob es sinnvoll ist, es wegzuwerfen. |
VERSUCH: 2. Wasserlöslichkeit
Durchführung: Füllt das Reagenzglas halbvoll mit Wasser. Gebt eine kleinere Menge (ewta 0,5 cm auf dem Spatel) eures Stoffes in das Wasser und schüttelt unter Verwendung des Gummistopfens. Überprüft, ob sich alles gelöst hat, oder ob noch Bodensatz vorhanden ist. Beobachtung: Nutzt die Begriffe löslich, unlöslich, Bodensatz zusammen mit Mengenangaben (wieviel Spatelspitzen), um die Löslichkeit zu beschreiben. Entsorgung: Die Lösung kann für Experiment 2 verwendet werden. |
VERSUCH: 3. pH-Wert der Lösung
Durchführung: Holt euch ein weiteres sauberes Reagenzglas, gebt soviel destilliertes Wasser wie im anderen Reagenzglas aus Experiment Nr. 2 hinein. Stellt die beiden Reagenzgläser nebeneinander in den Reagenzglasständer. Gebt nun vom sogenannte Universalindiktor in die Reagenzgläser, und zwar in beide gleich viele Tropfen. Die Farbe des Wasser dienst als Vergleichslösung, um die Färbung der Lösung beurteilen zu können. Ist die Farbe der Lösung ...
Entsorgung: In den Abfluss gießen, Reagenzgläser und Waschbecken gut mit Wasser ausspülen. |
| VERSUCH: 4. Betrachtung unter dem Mikroskop
Durchführung: Gebt ganz wenige Körnchen eures Stoffes auf eines der gelben Scheiben und stellt dann die Mikroskop-Kamera darüber eventuell kann man an dem großen, silbernen Drehrad an der Kamera das Bild etwas schärfer stellen. Beschreibt, was ihr seht:
Entsorgung: Kann weiter verwendet werden. Falls sich das Pulver über dem Tisch verteilt, bitte aufkehren und wegwerfen. Kristalle sind Körper, die aufgrund einer regelmäßigen Anordnung der kleinsten Teilchen glatte Flächen aufweisen |
| VERSUCH: 5. Verhalten bei Zugabe von Säure
Durchführung: Gebt etwa 0,5 cm eures Stoffes in ein sauberes Reagenzglas. Holt euch mit einem anderen Reagenzglas etwa 2 cm der Essigessenz (konzentrierter Essig), das ist unsere Säure. Gebt dann die Säure auf euren Stoff und beobachtet was passiert. Schwimmt der Stoff nur auf der Säure oder geht er unter? Oder bilden sich Bläschen, sobald die Säure mit eurem Stoff zusammenkommt. Entsorgung: Ins Waschbecken ausgießen und gut ausspülen. Eventuell mit einer Bürste Reste eures Stoffes entfernen. |
| VERSUCH: 6. Sonstige Beobachtungen
Haltet alles fest, was euch sonst noch an dem Stoff auffällt. Denkt aber daran, dass ihr hier keine Spekulationen äußert, sondern möglichst neutral festhaltet, was wahrgenommen wird. |
| Jeder Reinstoff zeichnet sich durch eine einzigartige Kombination von Stoffeigenschaften aus, anhand derer er identifiziert werden kann. Zwei Stoffe können nicht in allen Eigenschaften gleich sein. |
| Wir nutzen Stoffeigenschaften daher, um Stoffe zu identifizieren. |
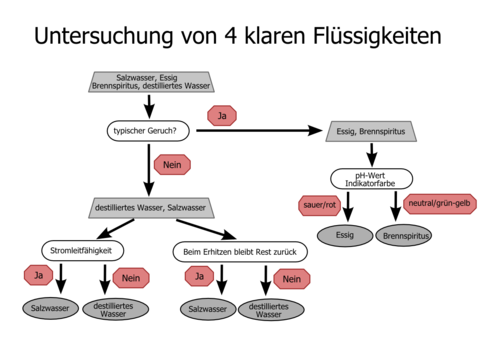
Fließschema zu Untersuchungen erstellen
Beispiel für 4 klare Flüssigkeiten
- 15px Anleitungs-Video zur Benutzung der Vorlagen und des Programms Inkscape
- Vorlagen für das eigene Fließschema: Quer-Format und Hoch-Format
Aus was bestehen wir ... und die Stoffe
Bisher haben wir die Stoffe und deren Eigenschaften betrachtet. Aber warum gibt es eigentlich verschiedene Stoffe mit verschiedene Eigenschaften? Um dahinter zu kommen, fangen wir mit einem überraschenden Experiment an, dass du zu Hause auch nachmachen kannst, denn man braucht nur recht alltägliche Stoffe, aber eine Möglichkeit zum genauen Messen von Volumen.
Zauberei ... es verschwindet etwas
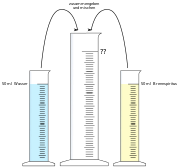
| VERSUCH:
Durchführung: Man misst in zwei Messzylindern jeweils 50 ml Wasser und 50 ml reinen Alkohol ab. Dann gibt man beide Flüssigkeiten zusammen und bestimmt das neue Volumen.
|
Nun, das Ergebnis verwundert die meisten und es wird vermutet, ob vielleicht etwas verschüttet wurde. Aber auch wenn man alles wiegen würde, so wäre nichts verschwunden.
Was das ist, die Materie, aus dem wir und alles um uns herum besteht, hat die Naturphilosophen schon vor 3000 Jahren beschäftigt.
Das Teilchenmodell gibt eine Erklärungsmöglichkeit
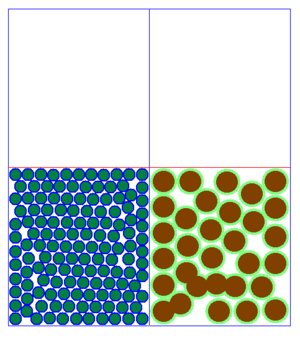
Die Forschung ist inzwischen soweit, dass sie ziemlich genau dieses Phänomen erklären kann. Tatsächlich ist es ein wenig komplizierter, aber vereinfacht ließe sich das Ergebnis erklären, wenn man davon ausgeht, dass beide Stoffe aus sehr kleinen Teilchen aufgebaut sind. Ist eines der Teilchen größer als das andere, so wird bei der Mischung Platz frei, denn die kleinen Teilchen nehmen Platz ein, der vorher unbesetzt war.
Diesen Vorgang wurde in einem Simulationsprogramm für Teilchen durchgeführt. Wie es abgelaufen ist kannst du dir noch einmal ausführlich in einem 15px Film (ohne Ton) anschauen.
Das Teilchenmodell früher und heute
Bereits vor etwa 2500 Jahren postulierte Demokrit Wie sein Lehrer Leukipp – und in Abweichung von dessen Lehrer Parmenides – dass die gesamte Natur aus kleinsten, unteilbaren Einheiten, den Atomen, zusammengesetzt sei. Davor galt die verbreitete Hypothese der unendlich fortsetzbaren Teilbarkeit der Materie. Zwar konnte um 1800 herum durch genaue Wägungen
Die Teilchen, aus denen unsere Materie aufgebaut ist, sind so klein, dass man sie mit keinem Mikroskop wirklich sehen kann. Bilder wie die folgenden sind Computer-Darstellungen, die aufgrund von Messungen in Elektronen- oder Rasterelektronenmikroskopen möglich sind. Solche Elektronenmikroskope erlauben trotzdem einen gewissen Einblick in die Welt der Teilchen, denn sie können die Anordnung der kleinsten Teilchen deutlich machen, ebenso wie Größenunterschiede, wenn man verschiedene Teilchen in der Probe hat.
aufnahme eines Gold-Kristalls. |
 |
Wie ein Rastertunnel-Mikroskop die Oberfläche abtastet ("rastert"). | ||
| 300px | 400px |
Grundregeln zum Teilchenmodell:
|
- WICHTIG: Man muss sich bewusst sein, dass das Teilchenmodell nur ein Hilfsmittel ist, den Aufbau der Materie und das Verhalten der Stoffe zu verstehen. Viele Dinge können damit nicht erklärt werden. Für uns reicht es aber im Moment, dieses einfache Teilchenmodell zu verwenden, mit dem wir dann auch verschiedene Aggregatzustände und die typischen Eigenschaften der Stoffe in einem bestimmten Aggregatzustand erklären können.
Häufig auftretende Fehler:
- Die Eigenschaften eines Stoffes ergeben sich erst aus der Anhäufung von mehreren Teilchen. Die Anziehung der Teilchen untereinander ist natürlich auch bei zwei Teilchen vorhanden.
- So hat ein kleinstes Teilchen keine Farbe. Die Farbe in den Elektronenmikroskop-Aufnahmen sind vom Computer erzeugt! Ein Farbeindruck entsteht dadurch, das ein Teil des weißen Licht durch den Gegenstand, den wir betrachten, verschluckt wird (Absorption). Das sichtbare Restlicht ergibt den Farbeindruck eines Gegenstandes (siehe 19px Remission ). Und einzelne Teilchen können kein Licht zurückwerfen, da sie zu klein sind.
Teilchenmodell anwenden und verstehen lernen
Es ist sicherlich schwer, etwas zu verstehen, was man ja eigentlich nicht sehen kann. Das Teilchenmodell kann aber in Simulationsprogrammen nachgestellt werden. Man kann dabei die Teilchen und deren Eigenschaften sowie die Eigenschaften der Umgebung festlegen. Als Hilfe zum Verstehen des Teilchenmodells nun ein paar Videos, zu denen es Kontrollfragen gibt. Frage nach, falls du Fragen falsch beantwortest und auch nicht verstehen kannst, warum es falsch ist.
| Schau dir den Film einmal an, bevor du die Fragen bearbeitest!
Schau dir die Teilchen an. Welche der drei Teilchen-Arten ziehen sich untereinander am stärksten an? (!Teilchen 1) (Teilchen 2) (!Teilchen 3) Welche Farbe hat der Stoff, in dem die Teilchen 3 enthalten sind? (!Gelb) (!Rot) (Kann man nicht sagen!) Müssen die Teilchen hier im Modell unterschiedlich groß sein? (Nein, denn es ist ja nur ein Modell, mit dem ich einige Eigenschaften verdeutlichen kann.) (!Ja, denn bei verschiedenen Stoffen hat man andere Teilchen) (!Die Größe der Teilchen ist sowieso nicht festgelegt und daher muss man hier auch nicht auf die Größe achten.) |
|
Wenn wir einen warmen Gegenstand anfassen, spüren wir an unserer Hand ... (die Reibung der Teilchen.) (!die Temperatur der Teilchen.) (!das der Stoff eine hohe Schmelztemperatur hat.) Wie kommt es, dass warmes Wasser seine Wärme an das Metall abgibt, dass ins Wasser eintaucht? (Die schnellen Wasserteilchen stoßen an die Metallteilchen an.) (!Das warme Wasser lässt das Metall schmelzen,, wodurch es warm wird.) Die Schieberegler-Skala geht nur bis 5 K, wobei das K für die Temperatureinheit 19px Kelvin steht. Man sagt, bei 0 K ist der absolute Nullpunkt und es gibt keine tieferen Temperaturen. Wie lässt sich das mit dem Teilchenmodell erklären? (!Es gibt keine Kühlgeräte, die stark genug sind.) (!Das ist eine physikalische Konstante und damit festgelegt.) (Bei 0 K stehen die Teilchen still. Langsamer geht nicht.) |
Teilchenmodell und Temperatur
Was wir in den zwei Videos gesehen haben und was durch die dazugehörigen Tests schon angesprochen wurde, wir nun noch mal in einem Lückentext betrachtet.
Die Bewegung der Teilchen ist eine Art von Energie (kinetische Energie), die der Stoff in sich aufnehmen kann. Die von außen zugeführte Energie lässt die Teilchen deshalb schneller bewegen. Umgekehrt, wenn eine Stoff abgekühlt wird, geben die Teilchen ihre Bewegungsenergie an die Umgebung weiter, indem sie andere Teilchen anstoßen und selber dabei langsamer werden. Der Verlust an Geschwindigkeit bedeutet einen Verlust an Energie und damit Wärme.
Dass die Teilchen sich bei einem heißen Stoff schneller bewegen, können wir mit der Hand spüren. Die schnelle Bewegung der Teilchen erzeugt Reibungswärme, die wir an der Hand fühlen. Bei einer kalten Oberfläche ist es eher umgekehrt. Die Teilchen in unser 37°C warmen Hand können die Teilchen des Stoffes in Bewegung bringen, wordurch dieser eine höhere Temperatur hat.
Wenn die Temperatur eines Stoffes mit der Geschwindigkeit der Teilchen zusammenhängt, dann ist es auch klar, warum man sagt, dass es einen absoluten Nullpunkt gibt. Denn wenn ein Stoff immer mehr abgekühlt wird, wird ja damit auch die Bewegung der Teilchen langsamer. Diese Abkühlung kann nur soweit gehen, bis die Teilchen (zumindest theoretisch) still stehen. Dies soll bei -273°C, oder auch 0 K der Fall sein.
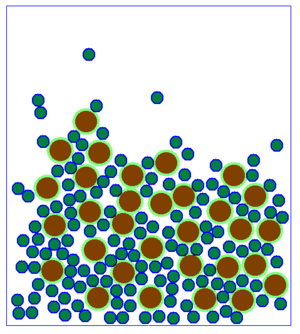
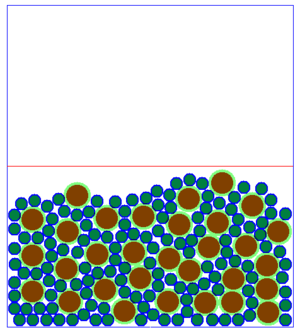
Viele Teilchen bei unterschiedlichen Temperaturen
Beobachtet man viele Teilchen auf einmal, so hat die Änderung der Geschwindigkeit auf jedes einzelne Teilchen den gleichen Effekt, wie auf ein einzelnes Teilchen, dass alleine ist. Allerdings sieht das Ganze dann etwas anders aus:
- Hinweis: Das die Teilchen nach unten fallen, bzw. sich eher weiter unten aufhalten hat damit zu tun, dass eine Schwerkraft simuliert wird. Wenn die ausgeschaltet wäre, würden auch langsame oder zusammenhängende Teilchen nicht "unten" liegen sondern herumschweben. Die Position der Teilchen hat also eher einen geringere Bedeutung.
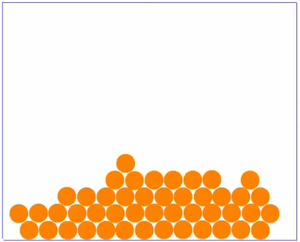
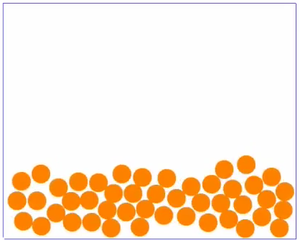
Es fällt auf, dass es beim Aussehen der Teilchenmenge deutliche Unterschiede gibt. Man kann im Grunde genommen drei verschiedene Arten der Anordnung der Teilchen festhalten.
 |
 |
 | ||
| Bei sehr niedrigen Temperaturen ist die Bewegung der Teilchen sehr langsam. Die Teilchen sind ganz nah beieinander, haben eine feste Position und bewegen sich nur wenig an ihrer Stelle. Dies ist möglich, weil wegen der langsamen Geschwindigkeit, die Anziehung zwischen den einzelnen Teilchen gut wirken kann. Ein Film, bei dem man Teilchen in Bewegung sieht findest du 15px hier. | Bei mittleren Temperaturen sind die Teilchen zwar auch recht eng beeinander, sind aber nicht - wie bei sehr niedrigen Temperaturen - fest an einer Stelle. Sie bewegen sich in aneinander vorbei, hin und wieder kann ein Teilchen mal die Gruppe verlassen. Da die Geschwindigkeit nicht so hoch wie bei den gasförmigen Soffen ist, kann die Anziehung zwischen den Teilchen etwas wirken, wodurch sie sich meist nicht voneinander entfernen können. Ein Film, bei dem man Teilchen in Bewegung sieht findest du 15px hier. | Bei sehr hohen Temperaturen sind die Teilchen sehr schnell. Sie ziehen sich natürlich immer noch an, aber wegen der schnellen Bewegung kann die Anziehung kaum wirken. So sind die Teilchen weit im Raum verteilt. Ein Film, bei dem man Teilchen in Bewegung sieht findest du 15px hier. |
Da diese drei Teilchen-Anordnungen von der Temperatur abhängen sollte es dir klar sein, dass wir hier sehen, wie die Teilchen bei Stoffen in unterschiedlichen Aggregatzuständen angeordnet sind. Das wollen wir uns noch etwas genauer anschauen und dann auch noch schriftlich festhalten.
Aggregatzustände im Teilchenmodell
Die drei Aggregatzustände haben wir schon behandelt. Wir wollen nun das Teilchenmodell auf sie anwenden und verstehen, wie die Existenz und die schon genannten Eigenschaften der kleinsten Teilchen die typischen Eigenschaften von festen, flüssigen und gasförmigen Stoffen erklärbar machen.
30px Aufgabe 12
Dazu vorab eine Übung, wo es um Stoffeigenschaften geht. Du findest unten einige Eigenschaften genannt, die du dem jeweiligen Aggregatzustand zuordnen sollst. Versuche die Eigenschaft richtig zuzuordnen. Diese Informationen sollen später bei der Aufgabe 3 in einer Tabelle festgehalten werden. Du kannst nach Abschluss dieser Übung schon anfangen, in die erste Spalte die zugeordneten Informationen in Stichworten beim jeweiligen Aggregatzustand festzuhalten. |
| Stoffe in festen Zustand | Das Volumen ist unveränderlich und ein Zusammendrücken ist nicht möglich. | Die Form des Stoffes ist unverändert, und er passt sich nicht an die Form eines Gefäßes an. | Der Stoff ist schwer verformbar | Der Stoff ist schwer teilbar. |
| Stoffe in flüssigen Zustand | Das Volumen ist so gut wie nicht veränderlich, denn in einer geschlossenen Sprite kann man den Stoff quasi nicht zusammendrücken. | Die Form ist veränderlich und der Stoff passt sich an die Form des Gefäßes an. | Der Stoff ist leicht teilbar. | |
| Stoffe in gasförmigen Zustand | Das Volumen ist veränderlich, denn in einer geschlossenen Spritze kann man den Stoff zusammendrücken. | Die Form ist veränderlich, denn der Stoff füllt ein Gefäß, gleich welcher Form, komplett aus. | Der Stoff verteilt sich von alleine im Raum. |
Nun geht es darum, wie man die Eigenschaften mit Hilfe des Teilchenmodell erklären kann.
30px Aufgabe 13
Ordne im Lückentext zu der jeweiligen Stoff-Eigenschaft eine Begründung mit Hilfe des Teilchenmodell zu. Als Anregung solltest du dir noch einmal die drei Bilder mit den orangenen Teilchen anschauen und die Beschreibung dazu durchlesen. |
Erklärung der Eigenschaften von festen Stoffen:
- Das Volumen ist unveränderlich und ein Zusammendrücken ist nicht möglich, weil die Teilchen schon ganz eng beieinander sind und nicht näher zusammenrücken können.
- Die Form des Stoffes ist unveränderbar, und er passt sich nicht an die Form eines Gefäßes an, da sich die Teilchen so stark anziehen können, dass sie immer an ihrer festen Position bleiben.
- Der Stoff ist schwer verformbar, denn aufgrund der großen Anziehung zwischen den Teilchen, bleiben sie an ihren Positionen und sind nicht verrückbar.
- Der Stoff ist schwer teilbar, da sich die Teilchen stark anziehen und man sie nur schwer trennen kann.
Erklärung der Eigenschaften von flüssigen Stoffen:
- Das Volumen ist so gut wie nicht veränderlich, denn in einer geschlossenen Spritze kann man den Stoff quasi nicht zusammendrücken, weil die Teilchen schon so eng beieinander sind, dass man sie so gut wie nicht weiter zusammendrücken kann.
- Die Form ist veränderlich und der Stoff passt sich an die Form des Gefäßes an, denn die Teilchen sind zwar nah beieinander und ziehen sich an, aber sie sind untereinander beweglich und halten nicht ihre Position.
- Der Stoff ist leicht teilbar, da die Anziehung der Teilchen nicht so stark ist, als das dies eine Trennung verhindern kann.
Erklärung der Eigenschaften von gasförmigen Stoffen:
- Das Volumen ist veränderlich, denn in einer geschlossenen Spritze kann man den Stoff zusammendrücken, was möglich ist, da die Teilchen normalerweise recht weit auseinander sind und man den Abstand verringern kann.
- Die Form ist veränderlich und der Stoff füllt ein Gefäß, gleich welcher Form, komplett aus, was man damit erklären kann, dass zwischen Teilchen kaum Anziehungskräfte herrschen und sie sich deshalb überall hin verteilen können.
- Der Stoff verteilt sich von alleine im Raum, wenn er nicht eingeschlossen ist, was man damit erklären kann, dass zwischen Teilchen kaum Anziehungskräfte herrschen und sie sich deshalb überall hin bewegen können.
30px Aufgabe 14
Nutze die leere Tabelle (odt, pdf und halte die Informationen aus den Übungen 1 und 2 fest.
|
30px Aufgabe 15
Auf dem Arbeitsblatt (pdf oder odt) sind einige Eigenschaften beschrieben, die nicht nur mit den Aggregatzuständen zu tun haben. Auch andere Eigenschaften von Stoffen lassen sich mit dem Teilchenmodell erklären. Nutze den freien Bereich in der Mitte, um den Satzanfang mit der Begründung zu verbinden.) |
In der Übung sind einige Dinge angesprochen worden, die du dir noch einmal in einem Film oder einer Animation anschauen kannst.
- Diffusion: Darunter versteht man einen natürlich ablaufenden Prozess, der mit der Zeit die vollständigen Durchmischung zweier oder mehrerer Stoffe durch die gleichmäßige Verteilung der beteiligten Teilchen bewirkt.
- Ein 15px englischer Film zeigt sehr ausführlich den Diffusions-Vorgang bei verschiedenen Gasen. Es wird auch gezeigt, wie sich unterschiedliche Temperaturen sich auf die Geschwindigkeit der Diffusion auswirken.
- Brown'sche Bewegung: Dabei handelt es sich um die Beobachtung des schottischen Botanikers Robert Brown im Jahr 1827, der unter dem Mikroskop beobachtete, wie Pollen in einem Wassertropfen unregelmäßig zuckende Bewegungen machten.
- Siedetemperatur: Da sich beim Sieden, also dem Übergang von flüssig zu gasförmig, die Teilchen eines Stoffes voneinander trennen müssen, ist die Stärke der Anziehung der Teilchen untereinander von wesentlicher Bedeutung. Teilchen mit starker Anziehung bedeuten für den Stoff, dass er eine hohe Siedetemperatur haben muss.
- Verdunstung: Wasser hat eine Siedetemperatur von 100°C. Trotzdem verschwindet es auch bei Temperaturen um 20°C in recht kurzer Zeit. Der Grund ist der, dass die Wasserteilchen sich zwar sehr stark anziehen, aber sehr leicht sind.
- In einem Simulationsivdeo siehst du zwei Teilchen, die die gleiche Anziehung haben, aber unterschiedlich schwer sind. DIe leichten Teilchen fliegen, wenn sie man aus Versehen die Menge verlassen, weiter als die schweren Teilchen.
- Löslichkeit: Stoffe, die man auflöst verschwinden scheinbar. Als Feststoff sind ja viele Teilchen eng beieinander. Nur deshalb kann man den Stoff überhaupt sehen. Im Wasser dagegen sind die Teilchen des Feststoffes voneinander getrennt und im Wasser verteilt. Da die einzelnen Teilchen zu klein sind, sieht amn sie nicht mehr.
- In einem Video wird der Lösungsvorgang simuliert.
Stoffe verändern sich - chemische Reaktionen
Wir haben die Eigenschaften von Stoffen untersucht und diese Stoffeigenschaften genutzt, um sie zu unterscheiden.
Es kann aber vorkommen, dass ein Stoff sich verändert, das er neue Eigenschaften bekommt. Das kann langsam gehen oder schnell:
- Eisen rostet mit der Zeit, es ist eine sehr langsame Veränderung, die unspektakulär ist.
- Magnesium verbrennt, wenn man es anzündet mit heller Flamme. Es bleibt ein weißes Pulver zurück.
30px Aufgabe 16
Überlege, warum wir davon ausgehen können, dass hier jeweils neue Stoffe entstanden sind. |
{{Kurzregel|Eine chemische Reaktion ist ein Vorgang bei dem Ausgangsstoffe verschwinden und neue Stoffe erscheinen. Dies kann man anhand der Eigenschaften erkennen.} }
- Magnesium vor und nach der Verbrennung
- Magnesium-products.jpg
Magnesium ist ein helles, silberglänzendes Metall.
- Magnesium ribbon burning.jpg
Wenn man es anzündet, brennt es mit sehr heller Flamme. Es steigt weißer Rauch auf was aber nur das verbrannte Magnesium ist, dass zurückbleibt, wenn die Flamme ausgegangen ist.
- Magnesium oxide.jpg
Weißer Rückstand der Magnesiumverbrennung.
| Chemische Reaktionen sind meist mit einem Umsatz an Energie verbunden. Es wird Energie frei oder man muss Energie hinzufügen. |
| Zusammenfassung: Eine chemische Reaktion ist ein Vorgang bei dem es zu einem Umsatz von Stoffen und Energie kommt. |
Dies soll noch einmal erklärt werden:
- Stoffumsatz: In diesem Fall bedeutet das, das die Ausgangsstoffe scheinbar verschwinden und dann stattdessen der neue Stoff vorhanden ist. Die Ausgangsstoffe werden also bei der chemischen Reaktion verbraucht.
- Energieumsatz: Dies kann unterschiedlich sein. Im Beispiel von bei der Verbrennung Magnesium heißt es, dass die Reaktion unter Energieabgabe stattfindet, auch wenn man am Anfang erhitzen muss, bis die Reaktion startet. Bei anderen Reaktionen muss man dauerhaft erhitzen, damit die Reaktion stattfindet. Beim Rosten von Eisen ist es eine sehr langsame Reaktion bei der auch Energie frei wird. Da die Reaktion aber langsam ist, merkt man keine Erwärmung.
30px Aufgabe 17
Fallen dir aus dem Alltag und im Haushalt chemische Reaktionen ein. Überlege jeweils und halte fest:
|
=== Was müsste bei einer chemischen Reaktion im Teilchenmodell passieren.
30px Aufgabe 18
|