Benzol und die Aromaten: Unterschied zwischen den Versionen
Aus Chemie digital
(→Energiestufen der Orbitale) |
(→Orbital-Modell bei Mehrfachbindungen) |
||
| Zeile 48: | Zeile 48: | ||
[[Datei:Elektronenkonfiguration leer kurz für Elektronen in Orbitalkästchen.png]] | [[Datei:Elektronenkonfiguration leer kurz für Elektronen in Orbitalkästchen.png]] | ||
| + | |||
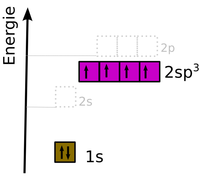
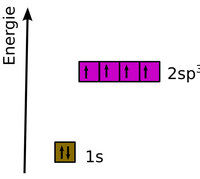
| + | === Hybridisierung === | ||
| + | |||
| + | [[Datei:EnergiestufenOrbitalmodellKohlenstoff1.png|200px]] [[Datei:EnergiestufenOrbitalmodellKohlenstoff2.png|200px]] [[Datei:EnergiestufenOrbitalmodellKohlenstoff3.png|200px]] [[Datei:EnergiestufenOrbitalmodellKohlenstoff4.png|200px]] | ||
| + | |||
=== Orbital-Modell bei Mehrfachbindungen === | === Orbital-Modell bei Mehrfachbindungen === | ||
Version vom 9. November 2016, 09:25 Uhr
Inhaltsverzeichnis |
Benzol und seine mysteriöse Struktur
Das Orbitalmodell als Erklärung für die merkwürdige Benzol-Struktur
Doppelspalt-Experiment:
- 01 Das Reich der Quanten und Elementarteilchen ... sehr ausführliches und gut erklärendes Video zum Doppelspaltxperiment bei Photonen.
- Das Mysterium - Quantenbewusstsein ... als Comic dargestellt, kürzer aber nicht so genau.
Filme auf dem Rheinland-Pfälzischen Omega-Server (nur mit Account nutzbar)
Elektronen als stehende Wellen in Elektronenschalen
- De Broglie gilt als einer der bedeutendsten Physiker des 20. Jahrhunderts, der für seine Entdeckung der Wellennatur des Elektrons (Welle-Teilchen-Dualismus) in seiner Dissertation 1929 den Nobelpreis für Physik erhielt.
Datei:Vibration corde trois modes petit.gif
Formen der Orbitale
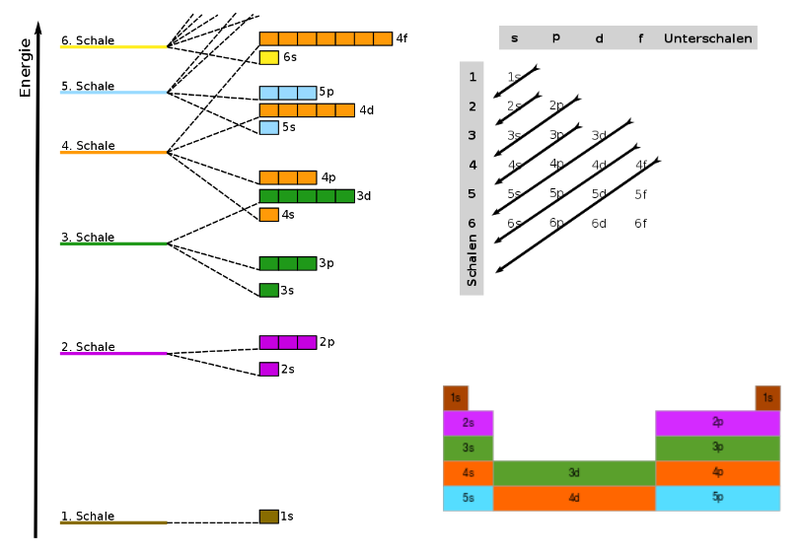
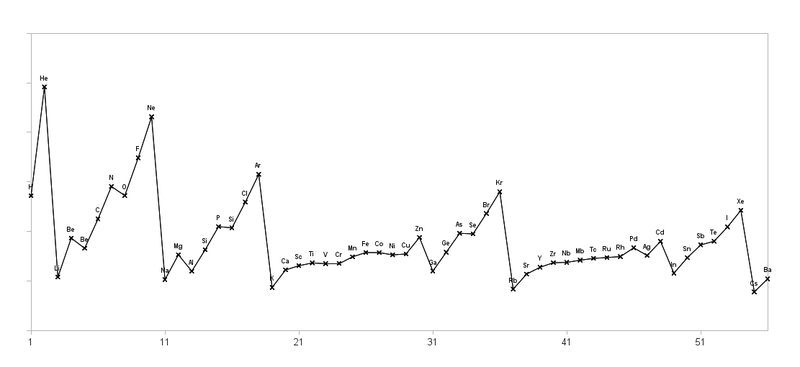
Energiestufen der Orbitale
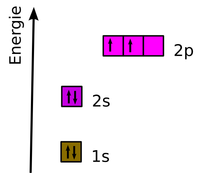
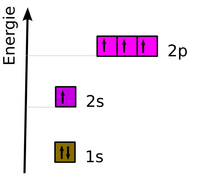
Beispiel für Elektronenkonfigurationen
Hybridisierung
Orbital-Modell bei Mehrfachbindungen
- Doppelbindung beim Ethen - Seite mit Erklärungen und Übungen usw.
- Bindungsverhältnisse im Benzol