Die Thermit-Reaktion im Schienenbau
Die Thermitreaktion im Schienenbau
Ein paar Eisenbahn-Fans haben netterweise im Rahmen einer Reihe von Filmen zur Gleisbautechnik auch einen wirklich guten Film zum Schweißen von Schienen erstellt und veröffentlicht.Wir schauen uns den Film mal an und versuchen herauszubkommen, welche chemische Reaktion da dahinter steckt.
|
Versuche das Reaktionsschema für die Thermitreaktion aufgrund der Informationen aus dem Film aufzustellen. |
Bei der Thermitreaktion handelt es sich wieder um Redoxreaktion. Das hast du mit geübtem Auge vielleicht schon erkannt und es ist ja auch im Film erwähnt worden. Wir wollen uns nun im folgenden darum kümmern wieder zu verstehen, warum sie funktioniert und - damit wir sie selber durchführen können - auch überlegen, wieviel der Edukte zusammengegeben werden müssen, damit ich ein stöchiometrisches Gemisch bekomme. Denn im Gegensatz zum Hochofen, wo das gasförmige Kohlenmonoxid den Hochofen einfach durchströmt und überall da hin kann wo es gebraucht wird, muss hier darauf geachtet werden, dass die Edukte gleich am Anfang im richtigen Verhältnis gemischt werden. Sonst läuft die Reaktion nämlich erst gar nicht ab.
Die Thermitreaktion in der Theorie - Energiebetrachtung
|
Stelle an der Reaktionsgleichung zur Thermitreaktion wieder fest ...
|
Bei unseren bisherigen Redoxreaktionen sind bisher immer Nichtmetalle (wie Kohlenstoff, Wasserstoff) oder Kohlenmonoxid als Reduktionsmittel eingesetzt worden. Die Aufgabe des Reduktionsmittel ist es unter anderem, die notwendige Energie für die Zerlegung des Metalloxids zu liefern, von dem wir das reine Metall haben wollen. Bei der Thermit-Reaktion wird nun Aluminium eingesetzt. Es ist dafür gut geeignet, da Aluminium ein recht unedles Metall ist und wir hatten schon vorher immer wieder festgestellt:
| Je unedler ein Metall ist, desto heftiger ist die Reaktion mit Sauerstoff. Es also viel Energie abgegeben. |
Ordnet man alle Metalle nach der Heftigkeit ihrer Reaktion, so bekommt man die sogenannte Redoxreihe der Metalle.
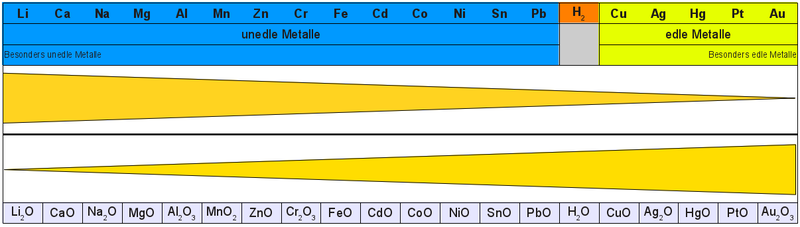
|
Ergänze die Zeichnung mit der Redoxreihe (hier zum Download auch mit mehr Platz) um Informationen um die Fähigkeit als Reduktionsmittel bzw. bei den entsprechenden Oxide um deren Fähigkeit als Oxidationsmittel zu wirken. Bei den Oxiden kannst du auch angeben, wie endotherm eine Zerlegung der entsprechenden Oxide ist. |
Betrachten wir die Thermit-Reaktion nun noch mal unter Verwendung der Redoxreihe der Metalle:
- Eisenoxid + Aluminium → Eisen + Alumniumoxid
- Aluminium ist ein unedleres Metall als Eisen.
- Bei der Oxidation von Aluminium wird mehr Energie frei als bei der Oxidation von Eisen.
- Für die Reduktion von Eisenoxid wird also umgekehrt weniger Energie benötigt, als bei der Oxidation von Aluminium frei wird.
- Deshalb kann Aluminium als Reduktionsmittel für Eisenoxid verwendet werden!
|
Überlege, welche der Redoxreaktionen möglich ist, indem du überlegst, welches der Metalle edler bzw. unedler ist. Gehe dabei folgendermaßen vor:
Zu dem Multiple-Choice-Test geht es hier! |
Die Thermitreaktion in der Theorie - Quantitative Betrachtung
Zur Erinnerung:
|
Damit die Thermitreaktion, die wir selber durchführen wollen auch wirklich abläuft, müssen wir möglichst genau wissen, wieviel Gramm vom Eisenoxid und wieviel Gramm vom Aluminium man zusammengeben muss.
Vom Gewicht her ist es zunächst einmal schwer die Antwort zu geben, aber wir betrachten zunächst nur die Atome bzw. Moleküle. Und da müssen wir nur zählen, dass kein Atom bei der Reaktion verschwindet oder dazu kommt.
|
Vorarbeit: Übersetze die systematischen Namen der beteiligten Edukte und Produkte in die Symbolschreibweise und trage es ins Heft ebenfalls untereinander ein:
|
Da wir nun wissen, aus was die Edukte und Produkte bestehen, können wir schauen, wieviele Atome wir brauchen.
|
Um dir das Malen und Zählen zu vereinfachen, gibt es ein interaktives Arbeitsblatt. Lies die Anleitung zum Arbeitsblatt, dass auf der externen Seite zu finden ist.
Schreibe, wenn du die ausgeglichene Reaktionsgleichung hast, diese in dein Heft ab unter der Überschrift: Reaktiongleichung zur Thermitreaktion in Symbolschreibweise.
|



