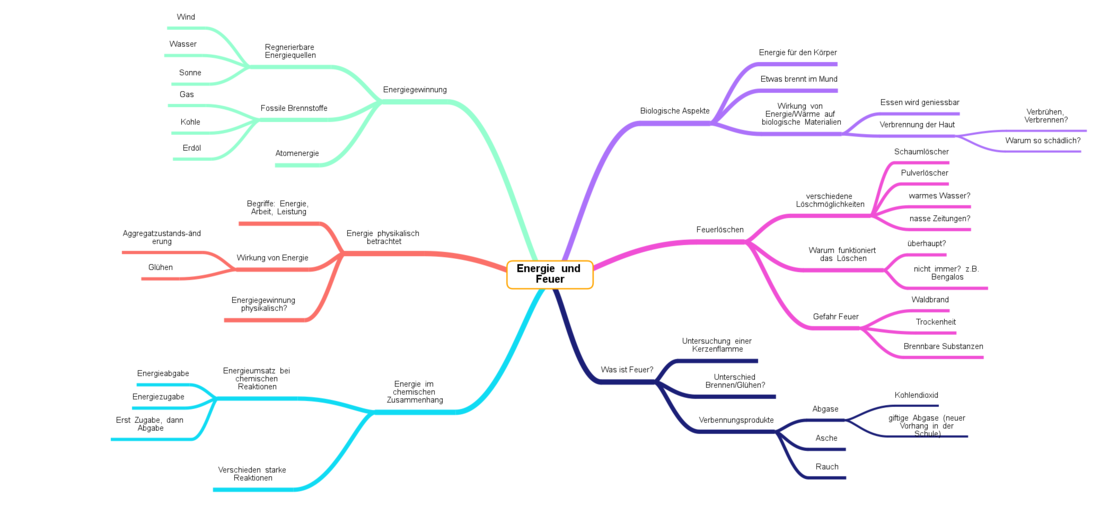
Feuer und Energie
Nachdem wir ein paar Ideen zum Thema gesucht haben, hier eine Übersicht der Themen, ein wenig sinnvoll sortiert.
Inhaltsverzeichnis |
Untersuchung einer Kerze und der Kerzenflamme
| 200px | Feuer und Energie gehören ja irgendwie zusammen, den Feuer ist eine typische Wärmequelle. Wir werden deshalb erst einmal einen alltägliche Vorgang betrachten, bei dem Energie frei wird.
Ihr sollte euch also eine brennende Kerze genauer anschauen. Dazu gibt es einige kleine Experiment, mit denen ihr erkennen könnt, was da beim Brennen passiert und was es so mit der Flamme auf sich hat. Nach den Experimenten schauen wir uns die Fachbegriffe und Informationen an und vergleichen Sie mit den Beobachtungen im Experiment. Dazu gibt es ein paar weiterführende Themen und interessante Fragen, die ihr mit dem neu erworbenen Wissen beantworten könnt. Alles weitere auf der Unterseite Brennen und Flamme. |
Energie aus physikalischer Sicht
| Bei Energie denkt man sicher zuerst an Strom. Sicher bekommt ihr mit, dass andauernd der Begriff Energie in den Nachrichten vorkommt: Energie sparen, Alternative Energie, fossile Energie, Sonnenenergie, ...
Für die Physiker ist der Begriff Energie von wichtiger Bedeutung. Auch wenn das Thema im Physik-Unterricht erst später durchgenommen wird, so solltet ihr vorab ein paar Dinge dazu wissen. Was ihr euch genauer anschauen sollt und ein paar Kontrollfragen gibt es auf der Unterseite Energie in der Pyhsik. |
Energieumsatz bei chemischen Reaktionen
Wichtige Vorgänge, bei denen der Energieumsatz eine wichtige Rolle spielt
- Die Photosynthese ist ein Prozess, bei dem Lichtenergie durch Lebewesen in chemische Energie umgewandelt wird und organische Stoffe synthetisiert werden. ... Die Synthese dieser Stoffe geht überwiegend von der sehr energiearmen anorganischen Kohlenstoff-Verbindung Kohlenstoffdioxid aus. Aus Kohlenstoffdioxid und Wasser entsteht – durch Energiezufuhr (Licht) – Traubenzucker (Glucose) und Sauerstoff.
Material 2: Chemische Energie
Verwendung chemischer Energie in technischen Systemen
- Aus technischer Sicht ist in Treibstoffen chemische Energie gespeichert, die durch deren Verbrennung, etwa beim Antrieb von Fahrzeugen, in mechanische Energie umgewandelt wird. Brennstoffzellen erlauben den Wandel von chemischen Reaktionsenergie einer Verbrennung direkt in elektrische Energie. Bei Nutzung von Batterien wird über elektrochemische Reaktionen die chemische Energie direkt in elektrische Energie gewandelt. Ein Akkumulator verhält sich bei der Nutzung der Energie ähnlich wie eine Batterie, kann aber auch umgekehrt elektrische Energie in chemische wandeln und so speichern.
Verwendung chemischer Energie in biologischen Systemen
- Aus biologischer Sicht ist in organischer Nahrung chemische Energie gespeichert, die in ATP als Energieträger umgewandelt wird. Grüne Pflanzen beziehen ihre chemische Energie nicht aus organischer Nahrung, sondern aus dem Energiegehalt der Sonnenstrahlung ...
Material 3: Bleiakku
- Bei einem Bleiakkumulator (kurz Bleiakku, besonders beim Kfz auch Starterbatterie) handelt es sich um eine Ausführung des Akkumulators, bei der die Elektroden aus Blei und der Elektrolyt aus verdünnter Schwefelsäure besteht.
- Bei der Entladung reagiert Blei mit Sauerstoff zu Bleioxid und löst sich im Elektrolyt auf. Beim Laden wird die Reaktion umgekehrt und es entsteht wieder metallisches Blei.
Material 4: Wasserstoff als Energieträger der Zukunft
- Wasserstoff scheint eines der Energieträger der Zukunft zu sein. Besonders sauber wird er hergestellt, wenn der für die Aufspaltung von Wasser in Wasserstoff und Sauerstoff benötigte Strom mit Hilfe von Solarzellen gewonnen wird.
- Wird das gasförmige Wasserstoff unter Druck verflüssigt, so kann man ihn auch in Tanks füllen und als Treibstoff verwendet werden. Dabei kann der Wasserstoff direkt mit Sauerstoff verbrannt werden oder die, in ihm enthaltene Energie, wird mit Hilfe einer sogenannten Brennstoffzelle in elektrischen Strom verwandelt werden. Und die „Abgase“? Als einziges Reaktionsprodukt entsteht Wasserdampf.
Informations-Quellen: Wikipedia-Artikel „Photosynthese“, „Chemische Energie“, „Bleiakku“, „Brennstoffzelle“
30px Aufgabe XX
Bei den in den Materialien beschriebenen Vorgängen finden immer auch chemische Reaktionen statt. Teilweise sogar zwei chemische Reaktionen. Bei allen ist die Umsetzung von Energie von großer Bedeutung.
|
Experimente zu Energie bei chemischen Reaktionen
Aus dem Buch hast du schon ein paar neue Begriffe zum Energieumsatz bei chemischen Reaktionen kennengelernt. Nun sollst du ein paar Reaktionen selber durchführen und dabei besonders auf die Umsetzung Energie achten. Einige Experimente gibt es nur als Videos.
| VERSUCH: Kupfersulfat und Wasser
Verwende bei beiden Versuchen eine Schutzbrille! ACHTUNG: 19px Kupfersulfat ist umweltgefährdend und darf deshalb nicht in den Abfluss! Hände nach dem Experiment waschen. Versuch 1: Erhitze in einem waagrecht eingespannten Reagenzglas etwas "blaues Kupfersulfat" (= Kupfersulfat-Hydrat). Beobachte die Farbe des Pulvers bzw. deren Veränderung und die Wand des Reagenzglases im nicht erhitzten Teil. Versuch 2: Versetze in einer kleinen Porzellanschale eine Spatelspitze weißes Kupfersulfat mit wenigen Wassertropfen aus der Plastikpipette und beobachte die Veränderung von Farbe und Temperatur! Nutze die aufgebauten Geräte und schaue dir noch einmal die Bilder an, die zeigen, wie das Experiment durchgeführt werden soll. Aufräumen: Gib das erhitzte bzw. mit Wasser versetzte Kupfersulfat jeweils in das passende Behältnis und "lege" wieder alle Geräte zurück. Ein Auswaschen ist notwendig. Es reicht die Reste aus zu schütten/klopfen/kratzen. |
| VERSUCH: Verschiedene Metallpulver verglühen lassen
Du sollst in diesem Experiment vergleichen, wie heftig die Reaktion verschiedener Metalle beim Verbrennen ist. Schutzbrille verwenden! Sind die Hände gewaschen? Dazu soll das Metallpulver in die Bunsenbrennerflamme gepustet werden. Gehe jeweils so vor:
Für jedes Metall sollte ein eigener Strohhalm vorhanden sein! Bitte geht sparsam mit dem Material um. Das Metallpulver ist nicht so sehr billig! Pro Metall sollten zwei Versuche mit kleinen Mengen reichen! Aufräumen: Kehrt den Bereich des Experimentes, damit kein Metallpulver mehr herumliegt. Schaltet den Bunsenbrenner ganz aus, wenn keine Gruppe direkt nach euch dran ist. |
| VERSUCH: Vergleich der Reaktion verschiedener Metalle mit Schwefel
Schau dir die folgenden Experimente an, bei denen Schwefel mit verschiedenen Metallen reagiert. Du findest auf den verlinkten Seiten jeweils den Film sowie noch einmal Bilder aus dem Film, wo die wichtigsten Momente noch einmal festgehalten sind. Es lohnt sich meist die Filme größere anzuschauen und auch die Bilder darunter noch einmal zu betrachten und die Erklärungen durchzulesen. |
| VERSUCH: Kettenreaktion
Betrachte dir dieses Video, in dem man eine Kettenreaktion beobachten kann. 15px
Überlege dir dazu folgendes und notiere es:
|
| VERSUCH: Zucker verbrennt mit Hilfe von Asche
Verwende bei beiden Versuchen eine Schutzbrille! Nimm eines der frischen Würfelzuckerstückchen. Versuch 1: Nutze den kleinen Gasbrenner und versuche den Zucker auf der unbrennbaren Unterfläche zu entzünden, indem du ihn stark erhitzt. Versuch 2: Gib nun etwas von der Asche auf das Zuckerstücken und versuche erneut den Zucker entzünden. Es sollte kein Haufen Asche sein, sondern dünn über die Zuckeroberfläche verteilt werden. Ein ähnliches Experiment kannst du dir 15px hier ansehen. Das solltest du auch tun, da man hier noch besser die Wirkung der Asche beobachten kann. |