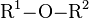Aktuelle Forschung zu neuen Treibstoffen
Aus Chemie digital
< Frau Lachner | Oberstufe neu
Version vom 1. März 2017, 18:53 Uhr von B.Lachner (Diskussion | Beiträge)
Inhaltsverzeichnis |
Power to Gas
Alkohole
Definition: ...
Benennung der Alkohole
Eigenschaften der Alkohole
Methanol der Supertreibstoff
- Oktanzahl: 160
- Dichte Methanol: 0,79 kg/l
Fragen:
- Wieviel CO2 entsteht aus einem Liter Methanol
- 1 l Methanol bringt wieviel Energie?
Ether
Definition: ...
Benennung Ether
Allgemein kann ein Ether als
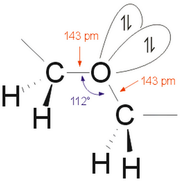
dargestellt werden. R1 und R2 sind hier Alkyl-Reste. Die Bindungsverhältnisse in Ethern ähneln denen in Alkoholen und im Wasser, das als Grundkörper dieser beiden Verbindungsklassen aufgefasst werden kann. Kohlenstoff- und Sauerstoff-Atome sind jeweils sp3 hybridisiert. Dies führt zu einer tetraedrischen Anordnung der Atomorbitale um alle beteiligten Atome. Der Bindungswinkel des Sauerstoffs ist aufgrund der gegenüber Wasserstoff (104,5° im H2O) voluminöseren Alkylsubstituenten mit 112° erweitert. Die C–O-Bindungen sind mit ca. 143 pm so lang wie in Alkoholen.
Entsprechend verläuft die Benennung der Alkoxy-Alkane. Beispiele:
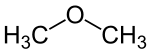
- Die Verbindung H3C–O–CH3 setzt sich zusammen aus einem H3C–O-Substituenten und dem Methyl-Rest (CH3) als Stamm, wobei hier allerdings beide Reste gleichwertig sind. Entsprechend heißt die Verbindung Methoxymethan oder Dimethylether:
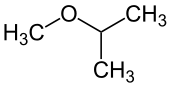
- H3C–O–CH(CH3)2 heißt 2-Methoxypropan oder Isopropylmethylether. Die höherrangige Propan-Kette bildet den Stammnamen, an die ein Methoxy-Substituent an 2- (bzw. iso-) Position des Propylrestes gebunden ist:
- FH2C–CH2–O–CH2-CH3 wird als 1-Ethoxy-2-fluorethan bezeichnet. Zwar sind beide Ketten prinzipiell gleichrangig, aber der fluorierte (und damit höher substituierte) Rest bildet den Namensstamm: