Moleküle und ihre Geometrie: Unterschied zwischen den Versionen
(→Bindungswinkel in der tetraedrischen Anordnung: table+) |
(→Regeln zur räumlichen Anordnung von Atomen in Molekülen: table+) |
||
| Zeile 41: | Zeile 41: | ||
=== Pseudostrukturen === | === Pseudostrukturen === | ||
| − | + | Die vier Kugelwolken, werden zwar meist "flach" dargestellt, tatsächlich aber verteilen sich die vier Kugelwolken gleichmäßig um den Kern herum. Sie haben dann eine sogenannte Tetraedrische Anordnung, wobei der Kern in der Mitte des Tetraeders liegt und die Kugelwolken kann man sich an den Ecken des Tetraeders vorstellen. Durch Doppelbindungen kann es aber auch zu anderen Anordnungen kommen, da man dann nicht vier "Anhängsel" sondern nur drei oder gar zwar hat. | |
| − | + | ||
| + | Unter der Beachtung der Regeln ergeben sich damit für eine bestimmte Anzahl an "Anhängsel" an einem Atom (ob Atom oder freies Elektronenpaar) mehrere sogenannte '''Pseudo-Strukturen'''. Man verwendet die Vorsilbe "Pseudo" für die nun folgenden Strukturen, weil freie Elektronen zwar Platz benötigen aber nur die Atome „sichtbar“ sind. Daraus ergeben sich die Realstrukturen, die im nächsten Abschnitt genauer betrachtet werden. | ||
{| class="wikitable " | {| class="wikitable " | ||
| Zeile 58: | Zeile 58: | ||
| [[File:AX1E0-3D-balls.png|100px]] | | [[File:AX1E0-3D-balls.png|100px]] | ||
| H<sub>2</sub> | | H<sub>2</sub> | ||
| − | | [[File:Wasserstoff.svg| | + | | [[File:Wasserstoff.svg|50px]] |
|- | |- | ||
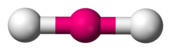
| − | | | + | | linear |
| − | | | + | | 180° |
| − | | | + | | [[File:AX2E0-3D-balls.png|170px]] |
| − | | | + | | CO<sub>2</sub> |
| − | | | + | | [[File:Carbon dioxide.svg|110px]] |
|- | |- | ||
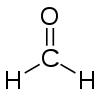
| − | | | + | | trigonal planar |
| − | | | + | | 120° |
| − | | | + | | [[File:AX3E0-3D-balls.png|150px]] |
| − | | | + | | Formaldehyd H<sub>2</sub>CO |
| − | | | + | | [[File:Formaldehyde-2D.svg|100px]] |
|- | |- | ||
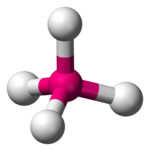
| − | | | + | | tetraedrisch |
| − | | | + | | 109,5 |
| − | | | + | | [[File:AX4E0-3D-balls.png|150px]] |
| − | | | + | | Methan CH<sub>4</sub> |
| − | | | + | | [[File:Methane-2D-stereo.svg|110px]] |
| + | |- | ||
| + | | ... | ||
| + | | ... | ||
| + | | ... | ||
| + | | ... | ||
| + | | ... | ||
| + | |- | ||
| + | | ... ''noch 5 weitere'' | ||
| + | | ... | ||
| + | | ... | ||
| + | | ... | ||
| + | | ... | ||
| + | |} | ||
| + | |||
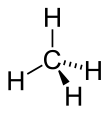
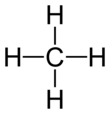
| + | [[File:Methane-2D-square.png|right|110px]]Wie bei der Lewisschreibweise von Methan kann man auch in einer "flachen" Darstellung andeuten, wie die räumlichen Anordnung ist. Man verwendet dazu Keile (''siehe Tabelle'') um anzudeuten, das etwa ein Atom oberhalb der Blattebene liegen müsste bzw. eine gestrichelte Linie, um zu verdeutlichen, dass das Atom hinter der Blattebene liegen müsste. Dies wird nicht immer gemacht und meist bei Methan die "flache" Darstellung (''siehe rechts'') verwendet, denn es wird vorausgesetzt, dass die Regeln zur räumlichen Anordnung bekannt sind. | ||
| + | |||
| + | |||
| + | === Reale Strukturen in der Tetraedrischen Anordnung === | ||
| + | |||
| + | |||
| + | |||
| + | Zunächst einmal eine Übersicht und dann folgen ein paar Erklärungen. In einer "mathematischen" Darstellung lassen sich die Strukturen [http://www.geogebratube.org/student/m31000 hier] von allen Seiten betrachten. | ||
| + | |||
| + | {| class="wikitable " | ||
| + | |- style="background: #DDFFDD;" | ||
| + | ! Pseudostruktur | ||
| + | ! Reale Struktur | ||
| + | ! Bezeichnung Reale Struktur | ||
| + | ! Berechneter Winkel | ||
| + | ! Beispiel | ||
| + | ! Beispiel in Lewisschreibweise | ||
| + | ! Tatsächlicher Winkel | ||
| + | |- | ||
| + | | [[File:AX4E0-3D-balls.png|110px]] | ||
| + | | [[File:AX4E0-3D-balls.png|110px]] | ||
| + | | tetraedrisch | ||
| + | | 109,5° | ||
| + | | Methan CH<sup>4</sup> | ||
| + | | [[File:Methane-2D-stereo.svg|110px]] | ||
| + | | 109,5° | ||
|- | |- | ||
| Element | | Element | ||
| Element | | Element | ||
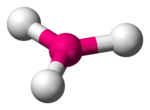
| + | | trigonal pyramidal | ||
| + | | 109,5° | ||
| + | | Ammoniak NH<sub>3</sub> | ||
| Element | | Element | ||
| − | | | + | | 107,8° |
| − | + | ||
|- | |- | ||
| Element | | Element | ||
| Element | | Element | ||
| + | | gewinkelt | ||
| + | | 109,5° | ||
| + | | Wasser H<sub>2</sub>O | ||
| Element | | Element | ||
| − | | | + | | 104,45° |
| − | + | ||
|- | |- | ||
| Element | | Element | ||
| Element | | Element | ||
| + | | linear | ||
| + | | 180° | ||
| + | | Fluorwasserstoff HF | ||
| Element | | Element | ||
| − | | | + | | 180°, ''aber eigentlich kein Winkel ablesbar!'' |
| − | + | ||
|} | |} | ||
| − | + | Entsprechendes lässt sich auf die anderen Pseudostrukturen übertragen. | |
| − | |||
| − | |||
[http://wikis.zum.de/chemie-digital/images/6/60/HF_bis_CH4.cml Avogadro-Zeichnung, um die Winkel zu messen] | [http://wikis.zum.de/chemie-digital/images/6/60/HF_bis_CH4.cml Avogadro-Zeichnung, um die Winkel zu messen] | ||
| − | {| | + | |
| − | + | {{Aufgabe|Ordne die bisher in Lewisschreibweise gezeichneten Moleküle den Pseudo- und Realstrukturen zu.}} | |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
Version vom 19. April 2013, 06:01 Uhr
Inhaltsverzeichnis |
Lewisschreibweise bei Verbindungen
Wichtige Begriffe:
|
|
Bestimme die Lewisschreibweise für die folgenden Verbindungen: H2S, NH3, HBr, AlCl3, Ethylen C2H2 |
Die letzten Aufgaben waren noch recht einfach, da man nur zwei Arten von Atomen hatte. Wenn 3 oder mehr Arten und vor allem auch eine größere Anzahl beteiligt ist, kann man leicht Fehler machen. In der letzten Aufgabe zeigte sich ein möglicher Fehler. Außerdem solltest du zur Kontrolle noch folgendes beachten:
Fehler die beim Zeichnen der Lewisschreibweise öfter sauftreten, sollten zur Sicherheit immer kontrolliert werden:
|
|
Nutze den Molekülbaukasten, um die Moleküle mit den folgenden Summenformeln zusammenzubauen und sie dann in Lewisschreibweise festzuhalten.
Tipp: Erst ein Molekül zusammenbauen, dann die Atome entsprechend der Anordnung im Modell ins Heft zeichnen, dann erst die Striche für die Bindungselektronen- und freien Elektronenpaare zeichnen, Abschlusskontrolle um Fehler auszuschließen. Lösung auf Extra-Seite |
Regeln zur räumlichen Anordnung von Atomen in Molekülen
Baut man eine Molekül mit dem Baukasten zusammen, so sieht man nicht nur, wie ein Molekül aufgebaut ist, sondern nebenbei auch noch die genaue räumliche Anordnung. Welches Winkel zwischen den Bindungen sind, ob ein Molekül ganz eben ist, wie etwa das Benzol, oder sogar ganz gestreckt.
Da dies bei der "flachen" Darstellung in der Lewisschreibweise verloren geht, muss man wissen, wo man welche Winkel hat ... und das lässt sich aus der Lewisschreibweise einigermaßen genau ablesen.
Dazu nun ein paar Regeln und Beispiele.
Grundregeln EPA (Elektronenpaarabstoßungsmodell):
|
Pseudostrukturen
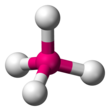
Die vier Kugelwolken, werden zwar meist "flach" dargestellt, tatsächlich aber verteilen sich die vier Kugelwolken gleichmäßig um den Kern herum. Sie haben dann eine sogenannte Tetraedrische Anordnung, wobei der Kern in der Mitte des Tetraeders liegt und die Kugelwolken kann man sich an den Ecken des Tetraeders vorstellen. Durch Doppelbindungen kann es aber auch zu anderen Anordnungen kommen, da man dann nicht vier "Anhängsel" sondern nur drei oder gar zwar hat.
Unter der Beachtung der Regeln ergeben sich damit für eine bestimmte Anzahl an "Anhängsel" an einem Atom (ob Atom oder freies Elektronenpaar) mehrere sogenannte Pseudo-Strukturen. Man verwendet die Vorsilbe "Pseudo" für die nun folgenden Strukturen, weil freie Elektronen zwar Platz benötigen aber nur die Atome „sichtbar“ sind. Daraus ergeben sich die Realstrukturen, die im nächsten Abschnitt genauer betrachtet werden.
Reale Strukturen in der Tetraedrischen Anordnung
Zunächst einmal eine Übersicht und dann folgen ein paar Erklärungen. In einer "mathematischen" Darstellung lassen sich die Strukturen hier von allen Seiten betrachten.
Entsprechendes lässt sich auf die anderen Pseudostrukturen übertragen.
Avogadro-Zeichnung, um die Winkel zu messen
|
Ordne die bisher in Lewisschreibweise gezeichneten Moleküle den Pseudo- und Realstrukturen zu. |