Mesomerie: Unterschied zwischen den Versionen
K (→Zusammenfassung) |
(→Vergleich der Reaktionen von verschiedenen Kohlenwasserstoff und Benzol mit Brom) |
||
| Zeile 47: | Zeile 47: | ||
* '''Addition''' bedeutet, dass in diesem Fall das Br<sub>2</sub>-Molekül zu dem Cyclohexen-Molekül dazu genommen wird. | * '''Addition''' bedeutet, dass in diesem Fall das Br<sub>2</sub>-Molekül zu dem Cyclohexen-Molekül dazu genommen wird. | ||
* Bei einer '''Substitution''' wird ein Teil des vorherigen Moleküls entfernt und durch einen Teil des Reaktionspartners ersetzt. Bei der Reaktion von Alkanen mit Brom, wird ein H im Alkan durch ein Br-Atom ersetzt. | * Bei einer '''Substitution''' wird ein Teil des vorherigen Moleküls entfernt und durch einen Teil des Reaktionspartners ersetzt. Bei der Reaktion von Alkanen mit Brom, wird ein H im Alkan durch ein Br-Atom ersetzt. | ||
| − | * '''Elektrophil''' bedeutet Elektronenliebend. Moleküle mit hoher Elektronendichte (Doppel- oder Dreifachbindung reagieren leicht mit Stoffen, die wenig Elektronen haben, manchmal auch als '''E<sup>+</sup>''' abgekürzt. | + | * '''Elektrophil''' bedeutet Elektronenliebend. Moleküle mit hoher Elektronendichte (Doppel- oder Dreifachbindung reagieren leicht mit Stoffen, die wenig Elektronen haben, manchmal auch als '''E<sup>+</sup>''' abgekürzt. Man nimmt als Beispiel häufig Brom als Reaktionspartner, wo das Elektrophil erst durch Trennung von Br<sub>2</sub> in Br<sup>+</sup> und Br<sup>-</sup> entsteht. |
| − | * '''Radikalisch''' kommt vom Begriff {{wpde|Radikal|Radikal}}, wo ein Atom ein ungepaartes Elektron hat. Meist entstehen Radikale durch den Einfluss von Licht oder leicht zersetzbaren | + | * '''Radikalisch''' kommt vom Begriff {{wpde|Radikal|Radikal}}, wo ein Atom ein ungepaartes Elektron hat. Meist entstehen Radikale durch den Einfluss von Licht oder leicht zersetzbaren Sauerstoffverbindungen. Bei einer radikalischen Reaktion sind Radikale als Zwischenstufen beteiligt.}} |
Auch beim {{wpde|Cyclohexen|Cyclohexen}} [[Datei:Cyclohexen - Cyclohexene.svg|30px]] findet, wie bei anderen Alkenen, eine Elektrophile Addition statt, was [http://chempage.alp.dillingen.de/organ/aromat/t12br6an.gif hier] auf dem Bild zu sehen ist. | Auch beim {{wpde|Cyclohexen|Cyclohexen}} [[Datei:Cyclohexen - Cyclohexene.svg|30px]] findet, wie bei anderen Alkenen, eine Elektrophile Addition statt, was [http://chempage.alp.dillingen.de/organ/aromat/t12br6an.gif hier] auf dem Bild zu sehen ist. | ||
Version vom 25. April 2012, 08:31 Uhr
Inhaltsverzeichnis |
Mesomerie am Beispiel des Benzols
Zusammenfassung
-
 Mesomerie hat man nur, wenn man abwechselnd Doppel- und Einfachbindungen hat (konjugierte Doppelbindungen, im Gegensatz zu
Mesomerie hat man nur, wenn man abwechselnd Doppel- und Einfachbindungen hat (konjugierte Doppelbindungen, im Gegensatz zu  kumuliert ).
kumuliert ).
- Das Molekül muss aber eben sein, damit sich die p-Orbitale überlappen können
- Bei ringförmigen Molekülen kann man auch Aromaten haben (Hückel-Regel)
- Die
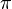 -Elektronen sind nicht in einzelnen Doppelbindungen lokalisiert sondern
-Elektronen sind nicht in einzelnen Doppelbindungen lokalisiert sondern  delokalisiert (verteilt) über mehrere Doppelbindungen.
delokalisiert (verteilt) über mehrere Doppelbindungen.
- Deshalb ist ein Stoff/Zustand mit Mesomerie energiearm (siehe Bild) und damit stabiler, d.h. er ist wenig reaktiv.
Warum wir uns mit Mesomerie beschäftigen
Die Mesomerie hat in vielen Bereichen der Chemie eine große Bedeutung, denn Sie hat Einfluss auf Eigenschaften und den Verlauf von chemischen Reaktionen. Durch gezielte Einflussnamen auf die Mesomiere kann man so auch ganz spezielle Produkte herstellen, ganz nach Wunsch.
Nun aber zu ein paar Beispielen der Anwendung ...
Phenol reagiert als Säure
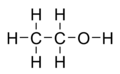
Die in Alkoholen enthaltene OH-Gruppe kann zwar H+ abgeben, aber dieser Zustand ist üblicherweise nicht sehr stabil, so dass man Alkohole im allgemeinen nicht als Säure bezeichnet.
Beispiel: Gibt Ethanol ein H+ ab, so entsteht das Ethanolat-Ion, dass aber bald wieder zurück zu Ethanol reagiert.
Beim ![]() Phenol (-ol wegen der enthaltenen Alkohol-Gruppe) dageben - früher auch unter dem Namen Karbolsäure bekannt - ist es etwas anders. Nach Abgabe eines H+-Ions bietet der Benzolring aufgrund der Mesomerie die Möglichkeit die negative Ladung zu verteilen.
Phenol (-ol wegen der enthaltenen Alkohol-Gruppe) dageben - früher auch unter dem Namen Karbolsäure bekannt - ist es etwas anders. Nach Abgabe eines H+-Ions bietet der Benzolring aufgrund der Mesomerie die Möglichkeit die negative Ladung zu verteilen.
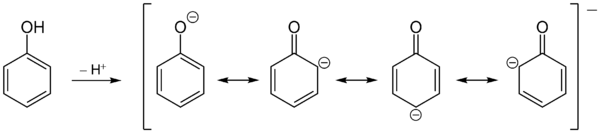
In der tatsächlichen Struktur ist dadurch die negative Ladung verteilt/delokalisiert und somit ist an den vier Stellen, an denen die Ladung in den Grenzstrukturen auftauchen kann, keine echte negative Ladung zu finden, sondern ... wenn man es vereinfacht formuliert ... nur 1/4 der negativen Ladung. Dadurch ist die Rückreaktion, also die Aufnahme des H+ nicht so leicht möglich und damit ist auch das Phenol/Phenolat-Gleichgewicht weiter nach rechts verschoben und man hat eine (immerhin) schwache Säure.
Vergleich der Reaktionen von verschiedenen Kohlenwasserstoff und Benzol mit Brom
In Klasse 11 haben wir uns mit den Reaktionen von Brom mit Alkanen und Alkenen beschäftigt.
- Alkane reagieren, bei ausreichend Licht, in einer
 Substitution Radikalischen Substitution .
Substitution Radikalischen Substitution .
- Alkene sind aufgrund der großen Elektronenkonzentration in der Doppelbindung reaktiver und reagieren quasi sofort mit Brom in einer
 Radikalischen Substitution .
Radikalischen Substitution .
Zur Erinnerung:
|
Auch beim ![]() Cyclohexen
Cyclohexen ![]() findet, wie bei anderen Alkenen, eine Elektrophile Addition statt, was hier auf dem Bild zu sehen ist.
findet, wie bei anderen Alkenen, eine Elektrophile Addition statt, was hier auf dem Bild zu sehen ist.
Anders beim Benzol, wo ich ja auch viele Elektronen in dem Pi-Elektronensystem habe. Hier findet kein Addition sondern eine Substitution statt. Mit ein Grund dafür, ist die Tatsache, dass eine der Zwischenstufen bei dieser ![]() aromatische Substitution Elektrophilen Aromatischen Substitution mesomeriestabilisiert ist, was im Folgenden Bild zu sehen ist.
aromatische Substitution Elektrophilen Aromatischen Substitution mesomeriestabilisiert ist, was im Folgenden Bild zu sehen ist.

Eine gute Erklärung, warum letztendlich keine Addition sondern eine Substitution stattfindet, könnt ihr auf dieser Seite nachlesen.
|
Versucht bei den folgenden Themen herauszusuchen, wie die Mesomerie einen Einfluss hat. Fasst zuerst zusammen um was es bei dem Thema geht und zeigt dann die Stelle, ab der sich die Mesomerie auswirkt. WICHTIG: Ihr sollt nicht einen Vortrag zu dem gesamten Thema halten. Konzentriert euch auf die Einleitungen, um über die Bedeutung etwas zu erfahren. Sucht dann die Stelle im Text, wo die Mesomerie vorkommt und versucht zu verstehen, welche Bedeutung hier die Mesomerie hat.
|